熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
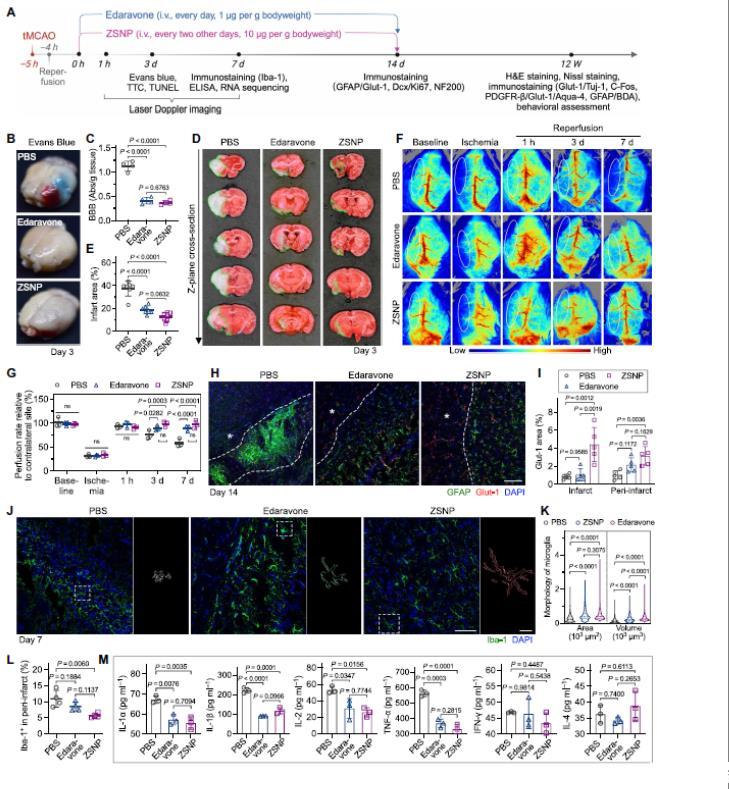
圖3. ZSNP減輕腦組織壞死并減弱缺血性中風(fēng)后的神經(jīng)炎癥激活。A. 實(shí)驗(yàn)設(shè)計(jì)示意圖。依達(dá)拉奉(每日1 μg g?1 體重)和ZSNP(每?jī)扇?0 μg g?1 體重)靜脈給藥14天。B. 和 C. 不同治療組tMCAO小鼠中風(fēng)區(qū)域伊文思藍(lán)外滲的代表性圖像(B)及分光光度法對(duì)每克腦組織伊文思藍(lán)的量化(C)(n=4只小鼠)。D. 和 E. 治療3天后,tMCAO小鼠各組TTC染色腦切片的代表性圖像(D)及相對(duì)梗死面積的量化(E)(n=7只小鼠)。綠色虛線圓圈表示梗死區(qū)域。F. 和 G. 代表性激光多普勒掃描圖(F)及腦血流灌注百分比的量化(G)(n=3只小鼠)。H. 各自治療14天后,缺血病灶內(nèi)及周?chē)腉FAP+星形膠質(zhì)細(xì)胞(綠色)和Glut-1+血管(紅色)的代表性免疫熒光圖像。白色星號(hào)表示梗死區(qū)域。I. Glut-1陽(yáng)性區(qū)域的相應(yīng)量化(每組n=5)。J. 治療7天后,缺血病灶內(nèi)及周?chē)鶬ba-1+小膠質(zhì)細(xì)胞的代表性免疫染色圖像。K. Iba-1+小膠質(zhì)細(xì)胞表面積和體積的量化(每組n=5)。L. 梗死周?chē)鷧^(qū)域Iba-1+小膠質(zhì)細(xì)胞相對(duì)面積的量化(每組n=5)。M. 中風(fēng)后第7天的炎癥細(xì)胞因子水平(n=3只小鼠)。
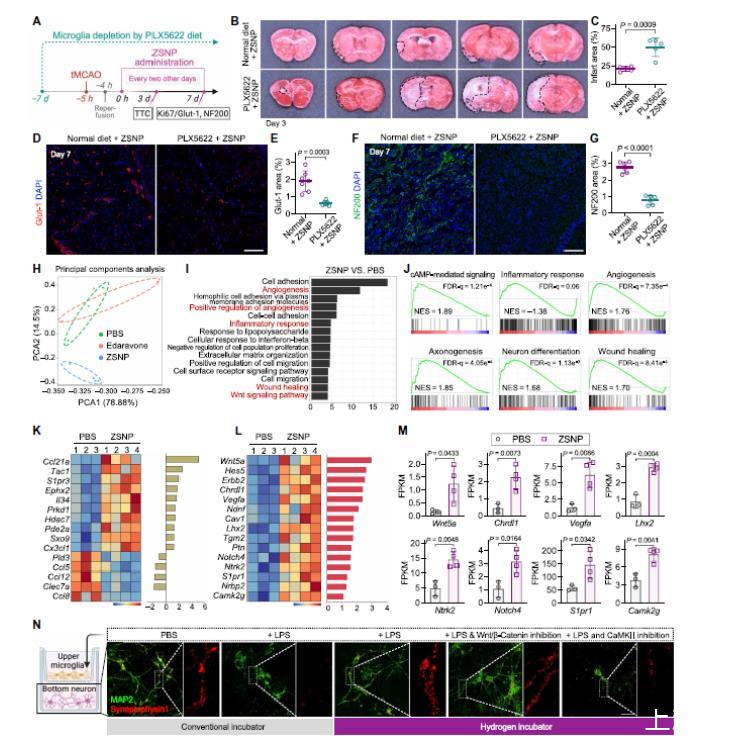
圖4、 ZSNP以依賴(lài)于小膠質(zhì)細(xì)胞的方式促進(jìn)缺血性腦修復(fù)。A. 小膠質(zhì)細(xì)胞清除實(shí)驗(yàn)的設(shè)計(jì)示意圖。B. 和 C. 小膠質(zhì)細(xì)胞清除對(duì)ZSNP療效影響的TTC染色代表性圖像(B)及梗死面積量化(C)(n=6只小鼠)。D. 和 E. Glut-1+血管長(zhǎng)入的代表性免疫熒光圖像(D)及其量化(E)(每組n=5)。F. 和 G. NF200+軸突發(fā)芽的代表性免疫熒光圖像(F)及其量化(G)(每組n=5)。H. 中風(fēng)后第7天從缺血腦中分離的小膠質(zhì)細(xì)胞的RNA測(cè)序數(shù)據(jù)主成分分析。I. ZSNP與PBS處理組間差異表達(dá)基因的基因本體論分析(生物過(guò)程)。J. ZSNP處理的小膠質(zhì)細(xì)胞的基因集富集分析圖。K. 和 L. 促炎基因(K)與腦修復(fù)相關(guān)基因(L)的表達(dá)熱圖。M. ZSNP調(diào)節(jié)的Wnt信號(hào)通路相關(guān)基因表達(dá)。N. 評(píng)估H2對(duì)小膠質(zhì)細(xì)胞-神經(jīng)元互作影響的體外共培養(yǎng)系統(tǒng)示意圖及結(jié)果。
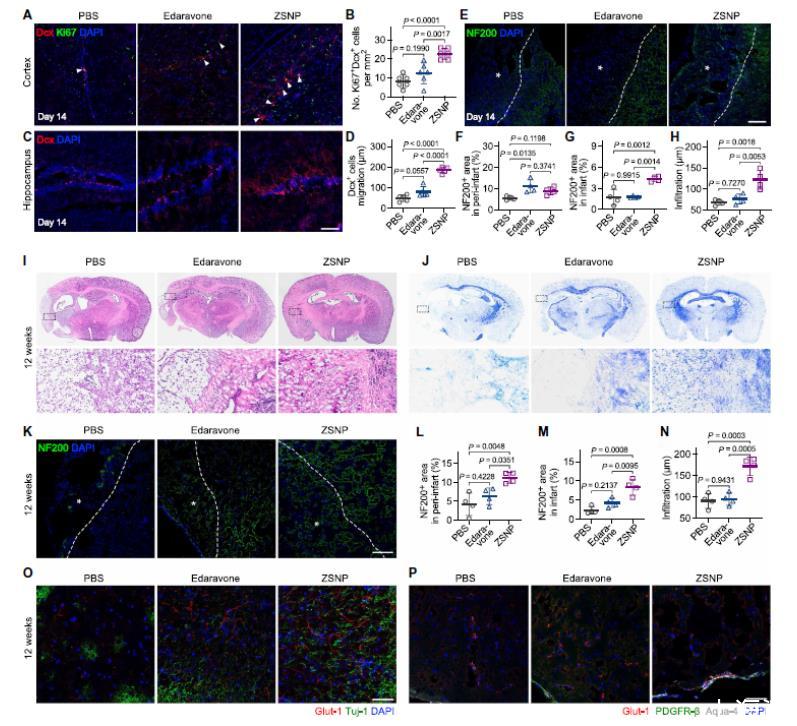
圖5. ZSNP誘導(dǎo)神經(jīng)發(fā)生和軸突發(fā)生。A. 和 B. 皮層中Ki67+/Dcx+增殖性神經(jīng)前體細(xì)胞的代表性免疫熒光圖像(A)及其數(shù)量量化(B)(每組n=5)。C. 和 D. 海馬Dcx+神經(jīng)前體細(xì)胞遷移的代表性圖像(C)及遷移距離量化(D)(每組n=5)。E. 至 H. 梗死及周邊區(qū)域NF200+軸突的代表性免疫染色(E)及其在梗死周邊區(qū)(F)和核心區(qū)(G)的密度量化,以及軸突向梗死組織穿透深度的量化(H)(每組n=5)。I. 和 J. 治療12周后腦組織的H&E染色(I)和尼氏染色(J)代表性圖像。K. 至 N. 治療12周后神經(jīng)絲蛋白面積的代表性免疫熒光圖像(K)及其在整體缺血半球(L)、梗死周邊區(qū)(M)和向梗死區(qū)浸潤(rùn)(N)的量化(每組n=5)。O. 血管(Glut-1,紅色)與軸突網(wǎng)絡(luò)(Tuj-1,綠色)空間關(guān)系的代表性共聚焦圖像。P. 顯示周細(xì)胞(PDGFR-β)和星形膠質(zhì)細(xì)胞終足(Aqua-4)覆蓋的成熟血管的代表性免疫染色圖像。
結(jié)論與展望
缺血性中風(fēng)再灌注后迫切需要安全高效的細(xì)胞保護(hù)策略,而目前的藥物療法尚無(wú)法滿足這一需求。納米技術(shù)在改善藥物向大腦遞送方面具有前景,但納米材料穿越血腦屏障(BBB)的效率非常有限,且納米材料在顱內(nèi)長(zhǎng)期滯留可能引發(fā)神經(jīng)毒性。本研究利用氫氣(H?)所具有的抗炎、穿透血腦屏障和生物安全性等特性,開(kāi)發(fā)了一種靶向/錨定于炎癥血管的產(chǎn)氫系統(tǒng)。通過(guò)將P-選擇素結(jié)合肽修飾到ZrSi?納米顆粒(ZSNP)表面,模擬了P-選擇素/P-選擇素糖蛋白配體介導(dǎo)的天然免疫招募機(jī)制。該設(shè)計(jì)無(wú)需依賴(lài)納米顆粒本身穿透進(jìn)入腦實(shí)質(zhì),而是使ZSNP錨定在血腦屏障的血管壁上,在此局部持續(xù)地通過(guò)水解反應(yīng)產(chǎn)生H?。釋放出的H?可穿過(guò)血腦屏障,通過(guò)抗氧化和免疫調(diào)節(jié)機(jī)制發(fā)揮細(xì)胞保護(hù)作用,協(xié)調(diào)多細(xì)胞修復(fù)過(guò)程。此外,ZSNP還能促進(jìn)小膠質(zhì)細(xì)胞介導(dǎo)的血管新生和神經(jīng)發(fā)生,引導(dǎo)軸突沿新生血管軌跡生長(zhǎng),并通過(guò)非經(jīng)典Wnt/Ca2?通路促進(jìn)小膠質(zhì)細(xì)胞-神經(jīng)元相互作用。這種神經(jīng)血管網(wǎng)絡(luò)的重建有助于功能性神經(jīng)回路的重新整合,從而實(shí)現(xiàn)超越依達(dá)拉奉(edaravone)的結(jié)構(gòu)與功能恢復(fù)。該策略通過(guò)在血腦屏障界面實(shí)現(xiàn)H?的持續(xù)釋放,而無(wú)需納米顆粒在顱內(nèi)蓄積,代表了一種有前景且負(fù)擔(dān)較低的缺血性中風(fēng)神經(jīng)保護(hù)新方法。Unisense微電極在本研究中扮演了不可或缺的定量檢測(cè)和驗(yàn)證角色,該設(shè)備能夠直接、實(shí)時(shí)地測(cè)量溶液中或生物組織內(nèi)溶解氫的濃度,為“ZSNP納米顆粒能否在目標(biāo)部位持續(xù)產(chǎn)生氫氣”這一核心問(wèn)題提供了客觀、定量的數(shù)據(jù)支持。Unisense微電極作為一種高靈敏度的原位檢測(cè)工具,通過(guò)提供體內(nèi)外氫氣濃度的直接定量數(shù)據(jù),有力地驗(yàn)證了作者提出的“血管錨定釋氫”策略的可行性,為整個(gè)研究的邏輯鏈條奠定了堅(jiān)實(shí)的實(shí)驗(yàn)基礎(chǔ)。
 相關(guān)新聞
相關(guān)新聞