熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
研究簡介:缺血性腦卒中是全球重大健康挑戰,盡管溶栓和取栓等再灌注療法已廣泛應用,但無法有效阻斷缺血再灌注引發的病理級聯反應。傳統神經保護藥物受限于血腦屏障(BBB)穿透性差、治療時間窗窄及潛在全身毒性等問題,臨床轉化效果不佳。納米技術雖為腦卒中治療帶來希望,但納米材料BBB穿透效率低下、顱內長期蓄積引發神經毒性等瓶頸仍亟待突破。針對上述難題,本研究開發了一種炎癥血管靶向錨定的氫氣(H?)控釋系統(ZSNP)。該系統以二硅化鋯(ZrSi?)納米顆粒為核心,通過P-選擇素結合肽(DAEWVDVS)表面修飾,模擬中性粒細胞與炎癥內皮細胞的天然黏附機制,實現對缺血病灶血管的主動靶向錨定。ZSNP無需跨越BBB,而是錨定于炎癥血管內皮,通過原位水解反應持續釋放H?,利用H?卓越的BBB穿透能力和組織擴散特性,實現腦深部遞送。研究通過3D細胞球體、微流控芯片及Transwell模型證實:ZSNP本身無法穿透生物屏障,但其釋放的H?可在15分鐘內快速跨越BBB,10分鐘即可在腦實質檢測到信號。與臨床常用自由基清除劑依達拉奉相比,ZSNP在抗炎、抗氧化方面表現出顯著優勢——ROS清除能力提升2.3倍,iNOS和γH2A.X表達分別降低1.3倍和1.6倍,同時精氨酸酶1(ARG1)水平上調2.4倍,有效促進小膠質細胞向修復表型轉化。在tMCAO小鼠模型中,ZSNP顯著減少腦梗死體積(較對照組降低69%),改善血腦屏障完整性,促進血管新生和神經發生。單細胞轉錄組測序揭示ZSNP通過非經典Wnt/Ca2?信號通路驅動小膠質細胞修復性極化,協調多細胞修復進程。長期隨訪顯示,ZSNP治療組軸突再生、神經環路重建及運動功能恢復均顯著優于依達拉奉,且12周后顱內納米顆粒完全清除,無蓄積毒性。該策略的創新性在于"以氣代固"的遞送理念——利用H?分子替代納米顆粒本身跨越BBB,既規避了納米材料的顱內蓄積風險,又實現了病灶部位的持續高濃度H?供給。這一"血管錨定-氣體釋放-屏障穿透"的三級遞送模式,為缺血性腦卒中的神經保護治療提供了安全高效的新范式,具有重要臨床轉化價值。
Unisense氫氣微電極系統的應用
Unisense氫氣微電極在該研究中主要用于定量檢測納米顆粒在體外和體內釋放的氫氣(H2)濃度,用于測量納米顆粒(ZSN和ZSNP)在去離子水中的氫氣釋放動力學。將H2微電極直接插入ZSNP溶液(100μg ml?1)中,在開放環境中實時測量溶解氫的濃度。這提供了氫氣釋放的連續動態曲線,并確定了峰值濃度。同步使用氫氣微電極在活體中風模型小鼠的腦部病灶處直接測量氫氣生成,首先在小鼠誘導缺血再灌注中風模型4小時后,靜脈注射ZSNP。隨后在小鼠顱骨缺血側鉆一個直徑0.8毫米的小孔,將H2微電極插入中風病灶處,分別在注射后的3、6、9、12和24小時定量檢測氫氣的產生量。
實驗結論
本研究成功構建了一種炎癥血管靶向的產氫納米系統(P-選擇素結合肽修飾的ZrSi?納米顆粒,ZSNP),該系統無需穿透血腦屏障即可在腦血管內皮表面錨定,并通過水解反應持續釋放氫氣(H?)。釋放的H?憑借其優異的擴散能力穿過血腦屏障,發揮抗氧化和免疫調節作用,有效減輕缺血再灌注損傷后的神經炎癥與氧化應激。更重要的是,該系統通過激活非經典Wnt/Ca2?信號通路,促進小膠質細胞與神經元之間的功能耦合,驅動小膠質細胞介導的血管新生與神經發生,并引導軸突沿新生血管定向生長,從而協同重建神經-血管網絡,實現結構與功能的雙重修復。相較于臨床藥物依達拉奉,該策略展現出更優的神經保護和恢復效果。由于ZSNP本身不進入腦實質,避免了納米材料在中樞神經系統的長期滯留和潛在神經毒性,同時利用氫氣的高生物安全性,整體策略具有良好的臨床轉化前景。
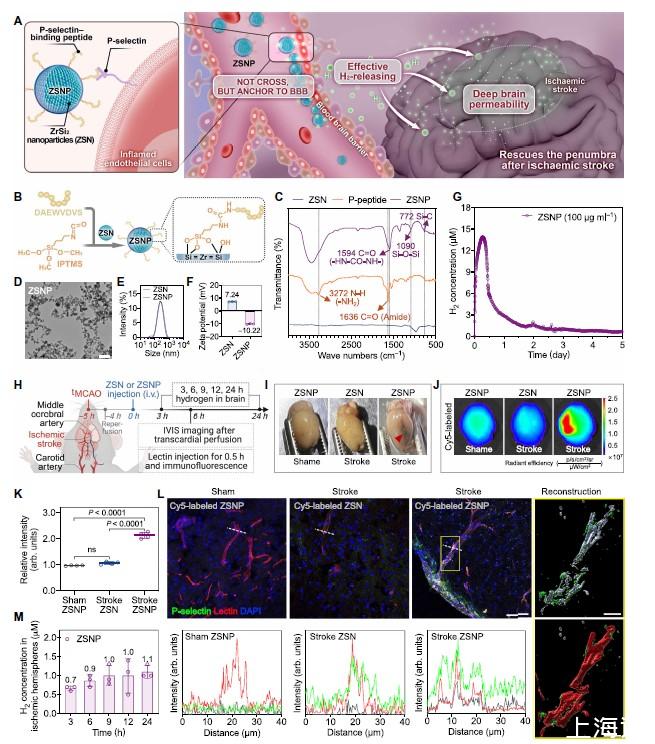
圖1、 發炎腦內皮錨定的釋氫納米顆粒的設計與表征。A)ZSNP治療缺血性中風的示意圖。ZSNP通過P-選擇素靶向發炎的腦血管,在血管處錨定并持續水解產生H2。H2自由擴散穿過血腦屏障,發揮神經保護作用,而納米顆粒本身不進入腦實質。B)ZSNP的合成路線示意圖。C) ZSN和ZSNP的傅里葉變換紅外光譜。D)ZSN和ZSNP的透射電子顯微鏡圖像。E) ZSN和ZSNP的動態光散射水合粒徑分布。F) ZSN和ZSNP的Zeta電位。G) ZSN和ZSNP的體外H2釋放曲線(n=3)。H) 體內靶向實驗的時間線示意圖。I) 注射后6小時,小鼠腦部的離體熒光圖像。Cy5標記的納米顆粒顯示為紅色。J) 圖I中缺血半球熒光信號的定量分析(n=4只小鼠)。K)中風模型與假手術模型中,ZSNP在腦部熒光信號的定量對比(n=4只小鼠)。L)(左)腦切片免疫熒光染色顯示Cy5-ZSNP(紅色)、P-選擇素(綠色)和凝集素標記的血管(白色)的共定位。(右)P-選擇素與凝集素雙染血管的3D重建圖像,顯示Cy5-ZSNP(紅色點)錨定其上。M)使用H2微電極在tMCAO小鼠缺血半球檢測到的H2濃度(n=3只小鼠)。
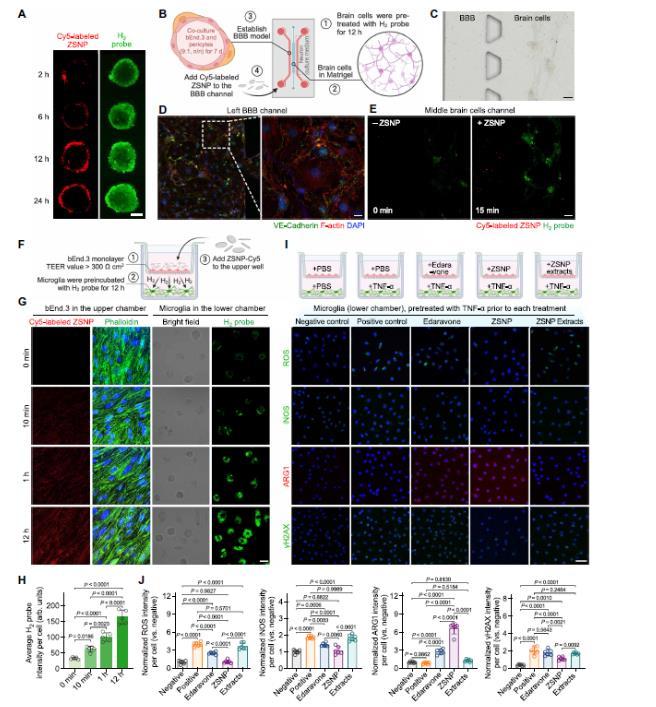
圖2. 從ZSNP釋放的H2穿過血腦屏障并發揮免疫調節作用。A. H2在間充質干細胞球中的時間依賴性滲透。B. 用于體外血腦屏障模型的微流控芯片設計示意圖。C. 微流控芯片中培養細胞的明場顯微鏡圖像。D. 左側血腦屏障通道中VE-鈣粘蛋白表達的免疫染色,證實了緊密連接的形成。E. 注射Cy5標記的ZSNP到左側血腦屏障通道15分鐘后,右側腦細胞通道中H2信號的共聚焦圖像。F. 體外Transwell血腦屏障模型的設計示意圖。G. 和 H. H2穿過Transwell血腦屏障模型的代表性共聚焦圖像(G)和定量分析(H)(每組n=5)。I. 下腔室中小膠質細胞的共聚焦圖像,針對炎癥相關生物標志物(ROS, iNOS, ARG1, yH2AX)染色。J. 圖I中生物標志物表達的相應定量分析(每組n=6)。