熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
還研究了傳質對SWASV響應的影響(攪拌與不攪拌)。常規SWASV測量在沉積步驟中使用攪拌來增加目標重金屬離子向電極的質量傳輸;然而,在不攪拌的條件下(模擬柑橘植物維管束內部),減少的質量傳輸可能成為Zn2+原位沉積的限制因素。圖7-5(b)顯示了不同微電極尖端尺寸在不攪拌條件下的校準曲線。對于85、48和12 μm的尖端尺寸,在不攪拌條件下,斜率和LOD受到嚴重影響。85、48、12和10 μm尖端尺寸的LOD分別增加了3,440%、1,710%、500%和80%。類似地,85和48 μm尖端尺寸的線性范圍也減小了,可能是由于質量傳輸限制,但12和10 μm尖端尺寸在攪拌和不攪拌條件下的線性范圍保持不變。表7-1比較了攪拌和不攪拌條件下的斜率、線性范圍和LOD。這些結果表明,與較大的尖端尺寸相比,質量傳輸限制對較小尺寸的影響較小。同樣明顯的是,凹陷增強了攪拌對電極響應的影響。例如,一個帶有凹陷的12 μm電極,在沉積過程中沒有攪拌時,其LOD增加了500%,但一個尺寸類似(10μm)沒有凹陷的電極并未顯示出LOD的顯著下降。這些發現與其他文獻一致(Bartlett等,2000),并且尤為重要,因為尖端尺寸較小的微電極可以減輕在預濃縮步驟中對攪拌的需求,從而實現原位測量。總體而言,在生物學應用中使用了一個在45-90 μm范圍內的鉍尖端尺寸(作為工作電極),以最小化質量傳輸干擾,并最大化LOD和斜率。
表7-1. 使用開發的鉍微電極,尖端尺寸對Zn2+的SWASV響應的質量傳輸干擾的影響
| 參數和條件 | 85 μm (無凹陷) | 48 μm (無凹陷) | 12 μm (有凹陷) | 10 μm (無凹陷) |
|---|---|---|---|---|
| 斜率 (μA/ppm Zn2+) | ||||
| 攪拌 | 0.1537 | 0.1073 | 0.0147 | 0.0012 |
| 不攪拌 | 0.0945 | 0.0527 | 0.0041 | 0.0011 |
| 變化百分比 | 38% | 50% | 72% | 8.3% |
| LOD* (ppm Zn2+) | ||||
| 攪拌 | <0.65 | 1.27 | 7.71 | 11 |
| 不攪拌 | 13.5 | 23 | 46.2 | 19.9 |
| 變化百分比 | -3440% | -1710% | -500% | -80% |
| 線性范圍 (ppm Zn2+) | ||||
| 攪拌 | >350 到 <0.65 | >350 到 1.27 | >350 到 7.71 | >350 到 19.9 |
| 不攪拌 | 145.4 到 13.5 | 268.3 到 23.0 | >350 到 46.2 | >350 到 19.9 |
| 變化 | 減小 | 減小 | 減小 | 相同 |
在柑橘植物維管束中使用SWASV原位檢測Zn2+
組合式鉍/鉑微電極被應用于柑橘植物維管束中的Zn2+檢測。雙管微電極的結構允許工作電極和參比電極同時穿透柑橘葉片的維管束,以進行Zn2+的SWASV測定。與單管鉍微電極相比,組合式鉍/鉑微電極顯示出更高的耐用性,并且未被葉片表面損壞。雙管鉍/鉑微電極的總尖端直徑為110 μm,工作鉍電極直徑為70 μm。校準曲線顯示對Zn2+具有優異的靈敏度,斜率為0.172 μA/ppm Zn2+,R2值為0.996(圖7-5(a))。應用于植物后的校準曲線顯示響應為0.187 μA/ ppm Zn2+,表明微電極在穿透過程中未被損壞。通過顯微鏡觀察,還發現與植物組織的直接接觸對微電極尖端沒有影響。前校準和后校準曲線(圖7-5(a))也顯示LOD為0.92 ppm,并且使用壽命研究表明電極的響應在18次使用中沒有變化(附錄E),這對于檢測植物中的Zn2+目的是可接受的。
圖7-5(b)顯示了微電極對經處理(1 mM ZnCl2處理6小時)和未處理(去離子水處理6小時)柑橘葉片中脈中Zn2+濃度的響應。兩片獨立的處理葉(1和2)產生的SWASV響應分別為1.2 μA(處理1)和1.4 μA(處理2),而兩片獨立的未處理葉片對Zn2+的響應(0.06 μA和0.003 μA)與處理葉相比可忽略不計。使用前校準和后校準曲線(圖7-5(a)),確定處理葉中含有5.73±0.88 ppm Zn2+,而未處理葉中含有不可檢測量的Zn2+。雖然處理葉中Zn2+濃度的增加是預期的,但由于使用了不同的分析方法,測量值難以用現有文獻驗證。大多數研究主要使用電感耦合等離子體原子發射光譜(ICP-AES)或原子吸收光譜(AAS)檢測Zn2+,這些方法需要將樣品干燥、研磨和消解后才能分析(1998)。這導致鋅濃度以每千克干重毫克數報告。一項使用更直接的鋅測量方法——微X射線熒光(μ-XRF)的研究報告了以毫克每千克干重為單位的Zn2+濃度(酸橙植物中為34.6至42.4 mg kg-1)(Tian等,2014)。考慮到μ-XRF測定的是總鋅濃度,并且干重測量(毫克Zn/千克生物質)和原位測量(毫克Zn2+/升)之間存在差異,使用原位SWASV的測量似乎是合理的。
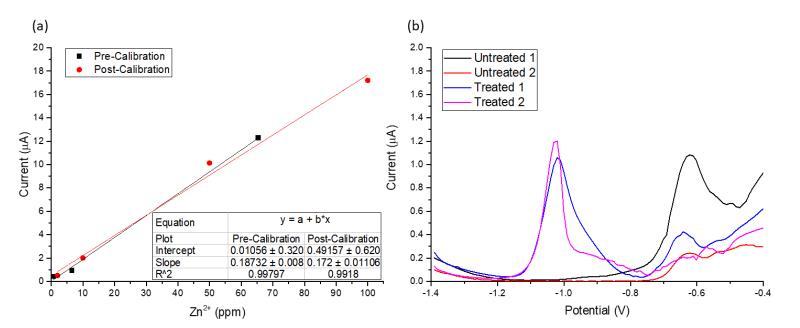
圖7-5. 開發的微電極在植物中的原位應用。(a)使用兩步SWASV方法的組合式鉍/鉑參比微電極的前校準和后校準曲線。(b)使用雙管鉍/鉑微電極在未處理(去離子水)和處理(1 mM ZnCl2)柑橘葉片中原位檢測Zn2+。
盡管使用基于SWASV的微電極監測柑橘植物中Zn2+濃度的好處是顯而易見的,但仍有一些局限性需要解決。特別是,已知在沉積步驟中會形成銅-鋅金屬間化合物,并干擾電極響應(Sanna等,2000)。然而,對金屬間Cu-Zn化合物干擾的量化超出了本文的范圍,因為假設柑橘葉片中的Cu2+濃度將顯著低于Zn2+(Sanna等,2000)。對于其他Zn2+和Cu2+同時以高濃度存在的應用,我們建議一種可能的解決方案是使用不同的沉積電位(例如,-0.6 V),該電位比還原Zn2+所需的電位更正,以確定Cu-Zn化合物的形成是否可能成為電極響應的問題。隨著在重現性和代表性方面更多的驗證,預計這種使用兩步SWASV的新方法將提供一種簡單、快速且可重現的植物中Zn2+檢測方法,能夠區分處理和未處理的樣品。總體而言,本研究證明了使用基于SWASV的微電極技術作為一種直接、快速的方法,以微創方式監測韌皮部組織中Zn2+濃度的可行性。
結論
構建了一種基于金屬鉍(Bi)的微電極,并對其用于檢測Zn2+的兩步SWASV概念進行了驗證測試。我們能夠證明使用Zn2+原位沉積和異位溶出的兩步SWASV測量的可行性。研究還發現,可以通過優化尖端尺寸來減少傳質限制并改善檢測限。隨后,將鉍微電極與鉑微電極組合成雙管微電極結構,用于直接測量植物中的Zn2+。我們的結果表明,Bi/Pt微電極的固體金屬尖端(直徑110 μm)足夠堅固,可以穿透柑橘葉片的厚表皮。總體而言,所開發的Bi/Pt微電極能夠對柑橘葉片中脈中的Zn2+產生響應,并能以高分辨率區分經Zn2+處理與未處理樣品之間的Zn2+濃度。這種新穎的原位檢測方法能夠直接在植物中追蹤其系統的Zn2+活性,這將有助于更好地理解其在植物中的潛在歸宿,從而在農業領域實現對HLB的有效管理。