熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
使用SWASV進(jìn)行微電極性能評(píng)估
為了將開發(fā)的雙管微電極應(yīng)用于植物系統(tǒng),對(duì)傳統(tǒng)SWASV進(jìn)行了修改,采用原位沉積和異位陽極溶出的兩步法(圖7-1)。首先,在含有不同濃度ZnCl2(0–300 ppm Zn2+)的Tris緩沖液(pH范圍5.0至7.5)中,將Zn2+沉積在鉍微電極上,以模擬植物環(huán)境。使用雙電極系統(tǒng),在攪拌和不攪拌兩種條件下,對(duì)鉍微電極施加相對(duì)于鉑參比電極為-1.4V的沉積電位,持續(xù)180秒。然后將微電極取出,用去離子水沖洗,并轉(zhuǎn)移到溶出溶液(不攪拌)中,在此使用恒電位儀(Palmsens3, Palmsens BV, Netherlands)進(jìn)行SWASV掃描(掃描:-1.4V 至 -0.4V;步進(jìn):10mV;振幅:40mV;頻率:5 Hz)以確定Zn2+濃度。在方波掃描期間,使用鉑網(wǎng)作為對(duì)電極,并使用Ag/AgCl電極(MI-401, Microelectrode Inc., Bedford, NH)作為參比電極。掃描后,通過在相同溶液中施加-0.4V電壓30秒來清潔微電極。
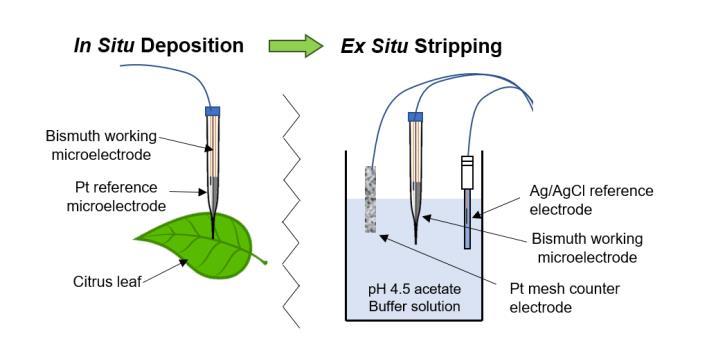
圖7-1. 在柑橘植物維管束中兩步SWASV測(cè)定Zn2+的概念圖。
在柑橘葉片中的原位應(yīng)用
在將開發(fā)的Bi/Pt微電極應(yīng)用于柑橘葉片之前,從酸橙幼苗上采集樣品葉,通過將葉柄浸入1 mM ZnCl2溶液中6小時(shí)來引入Zn2+。對(duì)照樣品暴露于去離子水中6小時(shí)。然后用去離子水沖洗所有葉片的表面,并用Kimwipe擦拭干。使用自動(dòng)三維(3D)微操作器(UNISENSE A/S, 丹麥)將組合式Bi/Pt微電極的尖端定位在中脈表面下400 μm處,用于Zn2+的原位沉積。pH微剖面和橫截面圖像的初步結(jié)果(附錄E)表明,大約300–400μm是柑橘幼苗韌皮部的典型深度。使用pH微電極(尖端直徑10 μm,UNISENSE A/S, 丹麥)和3D微操作器(UNISENSE A/S, 丹麥)進(jìn)行了局部原位pH測(cè)量。在Bi/Pt微電極的Bi側(cè)沉積Zn2+后,取出微電極,用去離子水沖洗,并使用自動(dòng)3D操作器將其轉(zhuǎn)移到陽極溶出溶液(0.1M醋酸緩沖液,pH 4.5)中。在移動(dòng)步驟中,使用帶CCD相機(jī)的立體顯微鏡(World Precision Instruments, Sarasota, FL)監(jiān)測(cè)微電極尖端的位置。使用恒電位儀(Palmsens3, Palmsens BV, Netherlands)進(jìn)行SWASV掃描,參數(shù)與校準(zhǔn)時(shí)使用的相同。所有實(shí)驗(yàn)均在法拉第籠(81-334-04, Technical Manufacturing Co., Peabody, MA)中進(jìn)行,以避免電干擾。為確保電極性能,進(jìn)行了使用前和使用后的校準(zhǔn)。
結(jié)果與討論
使用兩步SWASV進(jìn)行Zn2+檢測(cè)
陽極溶出分析的顯著靈敏度源于高效的預(yù)濃縮步驟與對(duì)累積金屬進(jìn)行靈敏的伏安溶出測(cè)量的結(jié)合。對(duì)于傳統(tǒng)的SWASV測(cè)量,預(yù)濃縮和溶出步驟發(fā)生在同一溶液中;然而,這不適用于柑橘樹的原位檢測(cè)。為了最小化在柑橘植物維管束內(nèi)進(jìn)行連續(xù)SWASV測(cè)量的影響,預(yù)濃縮步驟需要先使用一個(gè)組合的雙電極系統(tǒng)在原位單獨(dú)進(jìn)行,然后轉(zhuǎn)移到溶出溶液并連接到一個(gè)更靈敏的三電極系統(tǒng)。這一兩步過程使用鉍微電極進(jìn)行了評(píng)估,并與傳統(tǒng)的SWASV測(cè)量進(jìn)行了比較。對(duì)于常規(guī)測(cè)量,沉積步驟和溶出步驟均在pH 4.5的乙酸緩沖溶液(0.1 M)中進(jìn)行,使用鉑網(wǎng)對(duì)電極和Ag/AgCl參比電極。對(duì)于本研究中使用的改進(jìn)的兩步測(cè)量,沉積是在模擬植物系統(tǒng)的單獨(dú)Zn2+溶液(Tris緩沖液+ZnCl2)中進(jìn)行的,然后轉(zhuǎn)移到pH 4.5的乙酸緩沖液中進(jìn)行溶出。
圖7-2顯示了兩種方法之間響應(yīng)的差異。對(duì)于常規(guī)的SWASV測(cè)量,在200 ppm Zn2+濃度下觀察到的Zn2+峰高為0.022 μA。這顯著大于使用相同鉍微電極的兩步SWASV方法所得到的0.009 μA峰高。然而,研究發(fā)現(xiàn)兩種方法在1至200 ppm Zn2+濃度范圍內(nèi)都能表現(xiàn)出線性響應(yīng)。雖然常規(guī)SWASV測(cè)量對(duì)Zn2+顯示出更高的靈敏度(101 pA/ppm 對(duì)比 38 pA/ppm),但兩步法也能以優(yōu)異的線性響應(yīng)(R2=0.990)測(cè)量相關(guān)的Zn2+濃度。該結(jié)果首次表明兩步SWASV方法可以在植物系統(tǒng)中工作。
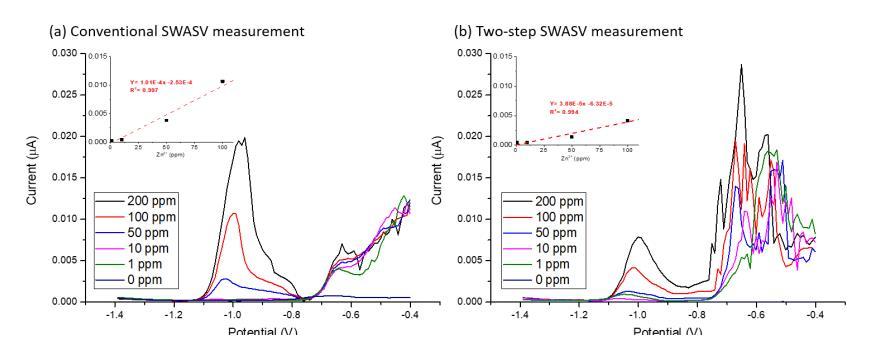
圖7-2. 開發(fā)的鉍微電極(尖端尺寸:直徑6 μm)對(duì)各種Zn2+濃度(1–200 ppm)的SWASV響應(yīng)對(duì)比:(a)常規(guī)方法:在pH 4.5乙酸緩沖液中沉積(攪拌)和溶出(不攪拌);(b)兩步SWASV方法:在ZnCl2溶液中沉積(不攪拌)并在pH 4.5乙酸緩沖液中溶出(不攪拌),溫度為23°C。插圖:1-100 ppm Zn2+的校準(zhǔn)曲線。
植物pH對(duì)微電極響應(yīng)的影響
使用兩步SWASV方法,在固定濃度為200 ppm Zn2+的去離子水溶液中,在pH 5.0至7.5的范圍內(nèi)研究了植物pH的影響(圖7-3)。使用HCl和NaOH調(diào)節(jié)pH。該pH范圍是柑橘植物維管束的典型范圍(Hijaz和Killiny 2014),本研究中也使用pH微電極進(jìn)行了測(cè)定(附錄E)。在最低pH(5.0)時(shí)獲得了最大的響應(yīng),為1.78 μA;然而,pH 5到6.5之間的響應(yīng)是可比的,范圍在1.40到1.78 μA之間。在pH 7.0時(shí),對(duì)Zn2+的響應(yīng)顯著下降了63%,峰值為0.66 μA,而pH 7.5時(shí)的響應(yīng)小于pH 5.0時(shí)電極信號(hào)的1%。這種隨著pH升高響應(yīng)下降的現(xiàn)象與Zn2+形態(tài)隨水溶液pH變化的情況一致。使用水化學(xué)模擬軟件(MINEQL)證實(shí),當(dāng)pH升高超過7.2時(shí),Zn2+的溶解度會(huì)降低。因此,開發(fā)的SWASV微電極很可能是在整個(gè)測(cè)試pH范圍內(nèi)對(duì)可溶性Zn2+濃度產(chǎn)生響應(yīng),并且當(dāng)pH升高到7.5時(shí),僅有少量可溶性Zn2+可供檢測(cè)。考慮到維管束的pH預(yù)計(jì)低于7,大部分鋅很可能通過使用鉍/鉑微電極開發(fā)的兩步SWASV方法檢測(cè)到。
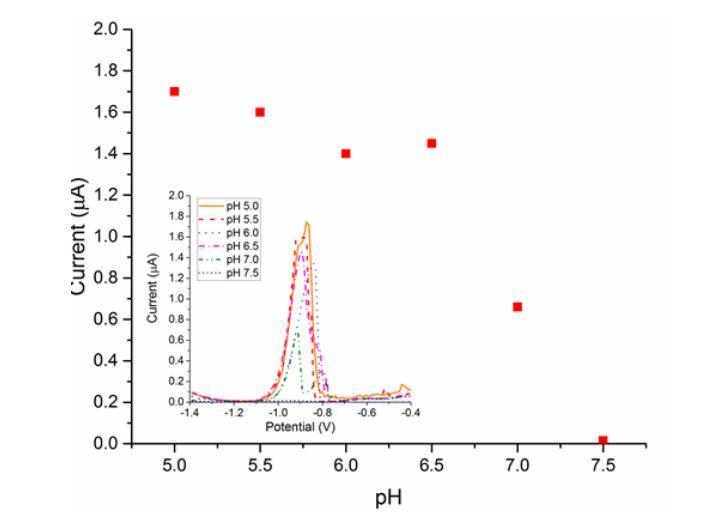
圖7-3. 預(yù)濃縮過程中pH對(duì)Zn2+濃度的SWASV響應(yīng)的影響(插圖:鉍微電極在不同預(yù)濃縮pH值下的SWASV伏安圖)。
尖端尺寸和傳質(zhì)對(duì)SWASV響應(yīng)的影響
SWASV對(duì)Zn2+濃度的響應(yīng)部分與工作電極的表面積有關(guān)。因此,研究了微電極尖端尺寸的影響,以優(yōu)化開發(fā)的鉍微電極用于柑橘植物的應(yīng)用。理想的尖端尺寸應(yīng)足夠小以穿透韌皮部,但又足夠大以對(duì)不同Zn2+濃度產(chǎn)生可區(qū)分的SWASV響應(yīng)。圖7-4(a)顯示了開發(fā)的鉍微電極在不同尖端尺寸(從10到85 μm)下的校準(zhǔn)曲線(附錄E)。正如預(yù)期,較大的尖端尺寸增加了SWASV響應(yīng)的靈敏度。例如,85 μm尖端尺寸的斜率為0.154 μA/ppm Zn2+,而10 μm尖端尺寸的斜率僅為0.0012 μA/ppm Zn2+。這些電極在單位表面積上表現(xiàn)出相似的靈敏度,平均歸一化靈敏度為每平方厘米1,246 ± 285 μA/ppm Zn2+。在攪拌條件下,85 μm尖端的LOD低于0.65 ppm Zn2+,而較小的尖端尺寸(例如,10 μm)具有較高的LOD(例如,~11 ppm Zn2+)。在攪拌條件下,微電極的凹陷對(duì)電極響應(yīng)沒有顯著影響(表7-1)。
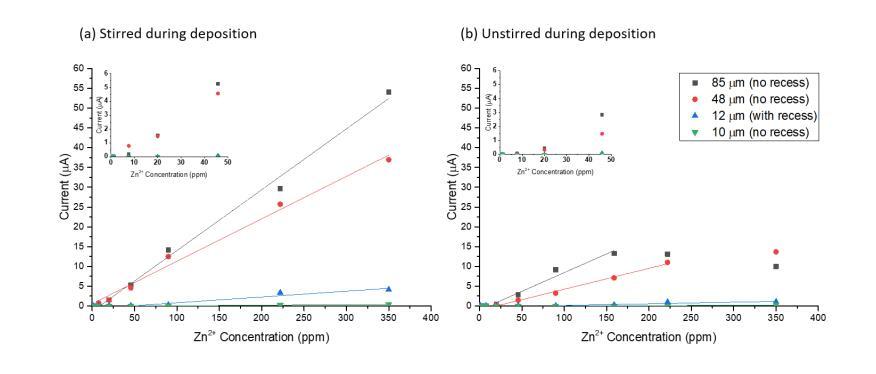
圖7-4. 傳質(zhì)對(duì)Zn2+檢測(cè)的影響:在沉積步驟中,不同尖端尺寸的鉍微電極在(a)攪拌和(b)不攪拌條件下的Zn2+ SWASV校準(zhǔn)曲線。插圖:電極在0到50 ppm Zn2+濃度范圍內(nèi)的響應(yīng)放大視圖。
 相關(guān)新聞
相關(guān)新聞