熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
H2 Treatment Attenuated Pain Behavior and Cytokine Release Through the HO-1/CO Pathway in a Rat Model of Neuropathic Pain
H2治療通過HO-1/CO通路減輕神經病理性疼痛大鼠模型中的疼痛行為和細胞因子釋放
來源:Inflammation, Volume 38, pages 1835–1846, (2015)
《炎癥》,第38卷,第1835–1846頁 , 2015年
摘要
本研究探討了氫氣(H2)治療在神經病理性疼痛大鼠模型中對疼痛行為和細胞因子釋放的影響及其機制。通過坐骨神經慢性壓迫損傷(CCI)誘導神經病理性疼痛,給予H2治療(腹腔注射富氫鹽水,每日10 mL/kg,持續7天)。結果顯示,H2顯著減輕了冷、熱和機械性痛覺過敏及異常性疼痛行為,并降低了背根神經節(DRG)和脊髓中促炎細胞因子TNF-α、IL-1β和HMGB1的釋放。此外,H2上調了血紅素氧合酶-1(HO-1)的mRNA和蛋白表達及活性,而HO-1抑制劑SnPP-IX逆轉了H2的鎮痛和抗炎作用。研究表明,H2通過激活HO-1/CO通路發揮抗痛覺過敏和抗炎作用。
研究目的
本研究旨在驗證H2治療是否通過HO-1/CO信號通路減輕神經病理性疼痛模型中的疼痛行為和炎癥反應,并闡明其分子機制。
研究思路
研究采用大鼠坐骨神經慢性壓迫損傷(CCI)模型模擬神經病理性疼痛。實驗分組包括假手術組、CCI組、CCI+H2治療組,并引入HO-1抑制劑SnPP-IX、誘導劑hemin和CO釋放分子CORM-2進行機制驗證。通過行為學測試(冷、熱、機械過敏評估)監測疼痛行為,ELISA法檢測DRG和脊髓中細胞因子水平,Western blot、RT-PCR和活性測定分析HO-1表達。使用丹麥Unisense氫氣傳感器確認富氫鹽水濃度,確保治療準確性。數據在術后1、4、7、10、14天采集,統計方法采用ANOVA。
測量的數據及研究意義
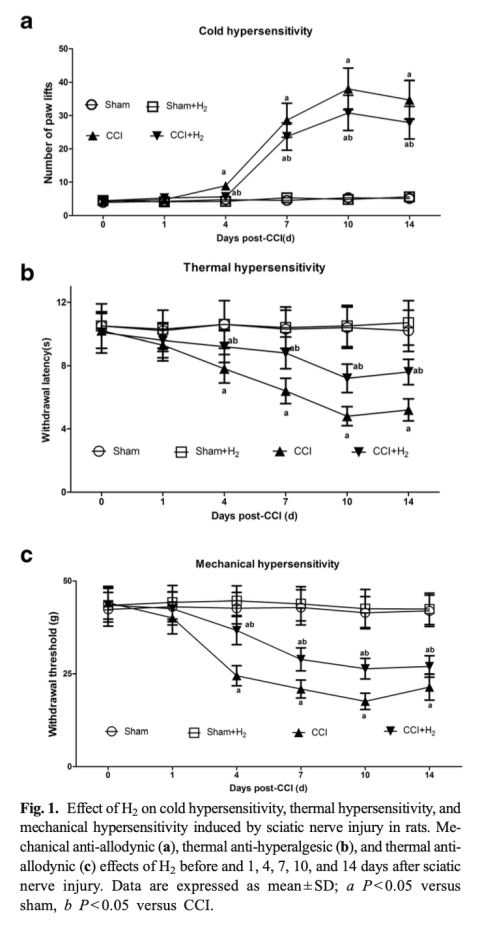
1 疼痛行為數據:來自圖1。測量了冷過敏(爪抬舉次數)、熱過敏(撤退潛伏期)和機械過敏(撤退閾值)。H2治療從第4天到第14天顯著改善所有疼痛行為,峰值效應在第10天。研究意義:直接證明H2具有鎮痛作用,為H2治療神經病理性疼痛提供行為學依據。
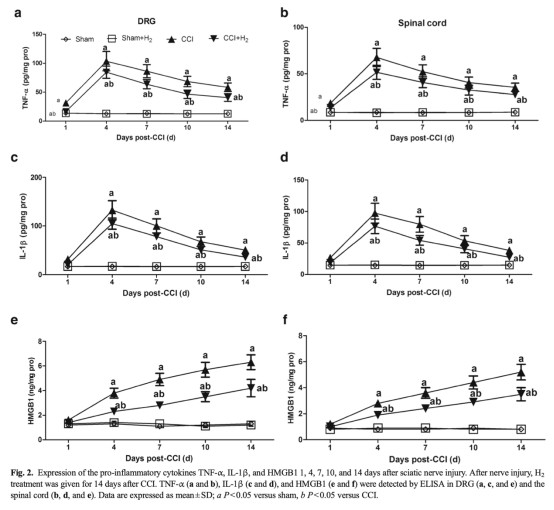
2 細胞因子釋放數據:來自圖2。檢測了DRG和脊髓中TNF-α、IL-1β和HMGB1水平。CCI誘導這些細胞因子升高,峰值在術后第4天(TNF-α、IL-1β)和第14天(HMGB1),H2治療顯著抑制其釋放。研究意義:表明H2通過抑制早期和晚期促炎細胞因子發揮抗炎作用,緩解神經炎癥。
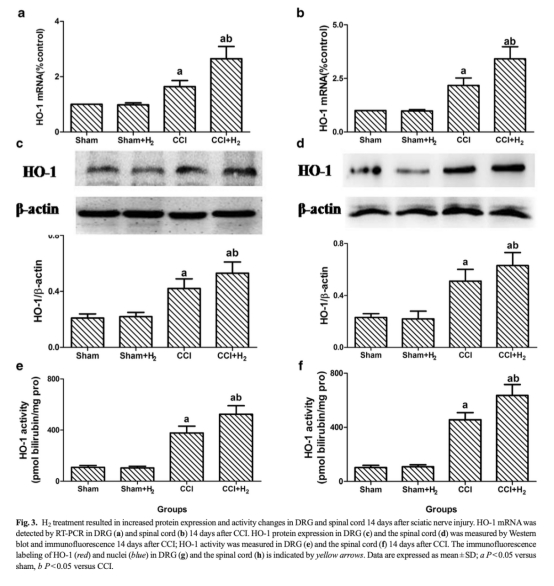
3 HO-1表達和活性數據:來自圖3和圖4。測量了HO-1 mRNA、蛋白表達和活性。CCI上調HO-1,H2進一步增強其表達和活性;SnPP-IX抑制H2效應,hemin和CORM-2協同增強。研究意義:驗證HO-1/CO通路是H2作用的關鍵機制,介導其抗痛和抗炎效果。
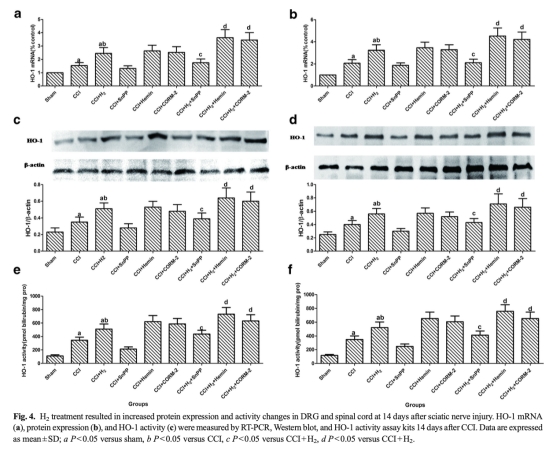
4 藥理學驗證數據:來自圖5和圖6。使用SnPP-IX(HO-1抑制劑)、hemin(HO-1誘導劑)和CORM-2(CO供體)干預。SnPP-IX逆轉H2的鎮痛和抗炎作用,hemin和CORM-2增強之。研究意義:確證H2效應依賴于HO-1/CO通路激活,為靶向治療提供理論支持。
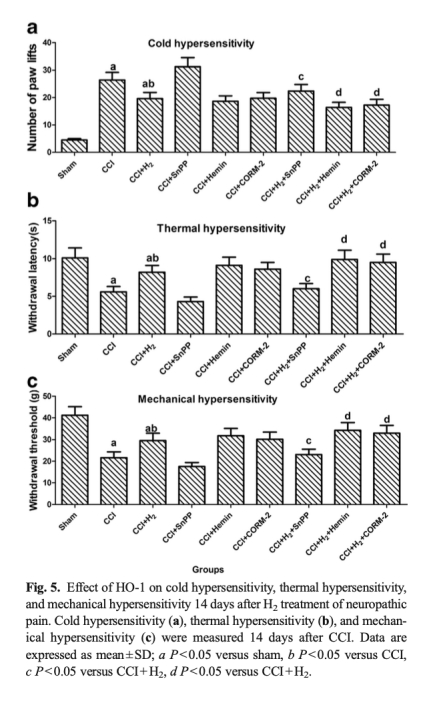
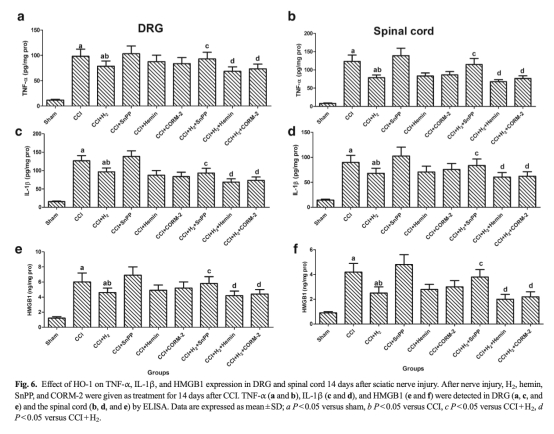
結論
1 H2治療通過上調HO-1表達和活性,激活CO信號,顯著減輕神經病理性疼痛的行為學表現(痛覺過敏和異常性疼痛)。
2 H2抑制DRG和脊髓中促炎細胞因子(TNF-α、IL-1β、HMGB1)的釋放,發揮抗炎作用,該效應可被HO-1抑制劑阻斷。
3 HO-1/CO通路是H2鎮痛和抗炎的核心機制,提示H2作為神經病理性疼痛的潛在治療策略。
使用丹麥Unisense電極測量數據的研究意義
本研究使用丹麥Unisense A/S公司生產的針型氫氣傳感器(needle-type hydrogen sensor)測量富氫鹽水中的氫氣濃度,以確認治療溶液的H2含量。該傳感器具有高靈敏度和特異性,可實時檢測溶解氫水平,確保實驗中使用H2濃度的準確性和一致性(文檔中提及H2濃度達到0.6 mmol/L)。研究意義在于:第一,該方法標準化了H2給藥條件,排除濃度偏差對結果的干擾,保證實驗可重復性;第二,Unisense傳感器提供的定量數據驗證了富氫鹽水的制備質量,為H2治療的可信度提供技術支撐;第三,通過精確控制H2劑量,強化了H2通過HO-1/CO通路起作用的因果關系,避免了因H2濃度不均導致的假陽性或假陰性結果。總之,該測量手段提升了研究的嚴謹性,為H2的轉化應用奠定了基礎。