熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Optimized Real-Time Monitoring of Glutathione Redox Status in Single Pyramidal Neurons in Organotypic Hippocampal Slices during Oxygen-Glucose Deprivation and Reperfusion
優化實時監測器官型海馬切片中單個錐體神經元在氧糖剝奪和再灌注期間的谷胱甘肽氧化還原狀態
來源:ACS Chemical Neuroscience, 6, 2015, 1838?1848
《ACS化學神經科學》,第6卷,2015年,第1838?1848頁
摘要:
摘要描述了研究通過轉染Grx1-roGFP2融合蛋白到器官型海馬切片培養(OHSCs)的CA1區錐體神經元中,實時監測氧糖剝奪和再灌注(OGD/RP)過程中谷胱甘肽(GSH)系統的變化。研究優化了灌注系統,確保pO2變化與體內中風模型時間尺度一致,并使用tdTomato作為內部標準改進校準。結果顯示,在線粒體中,GSH系統在OGD期間變得更還原,在RP期間更氧化,而細胞質中沒有顯著變化。
研究目的:
研究目的是開發一種優化方法來實時監測腦卒中體外模型(OGD/RP)中GSH氧化還原狀態的變化,特別是在單神經元水平,以理解氧化應激在神經元損傷中的作用。
研究思路:
研究思路包括:首先,通過基因槍或單細胞電穿孔轉染cyto-或mito-Grx1-roGFP2到OHSCs的錐體神經元中, targeting cells in a narrow depth range;其次,優化灌注系統(如[O+V]系統)以實現快速、可重復的溶液交換,模擬體內pO2變化;然后,使用丹麥Unisense電極測量pO2隨深度和時間的變化;最后,利用tdTomato校準Grx1-roGFP2信號,定量分析氧化還原參數(如OxDroGFP2和E_GSH),并應用于OGD/RP協議。
測量的數據及研究意義:
1. 測量了pO2在不同灌注系統中的變化(圖1),研究意義是驗證了優化系統[O+V]能快速控制pO2,確保實驗條件與體內中風模型可比,提高了模擬的可靠性。
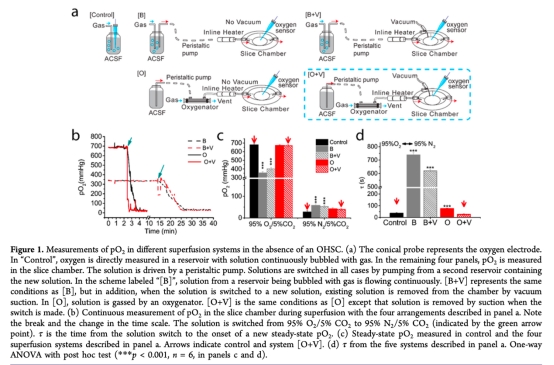
2. 測量了pO2隨OHSC深度的變化(圖2),研究意義是確定了轉染細胞所在深度范圍(30-45μm)的pO2可控且一致,為單神經元測量提供了可重復的環境。
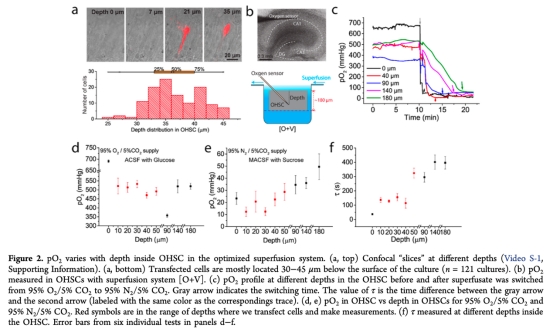
3. 測量了mito-Grx1-roGFP2信號與pO2變化的同步性(圖3),研究意義是證實了傳感器能快速響應OGD/RP過程中的氧化還原變化,驗證了方法的實時性。
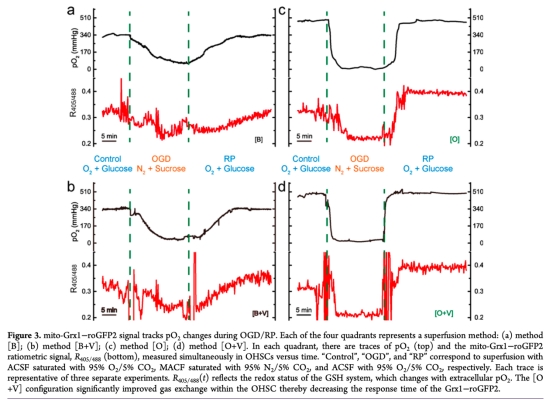
4. 測量了tdTomato作為內部標準校準Grx1-roGFP2的效果(圖4),研究意義是解決了OGD/RP后細胞形態變化對熒光信號的干擾,使氧化還原參數(如OxDroGFP2)的定量更準確。
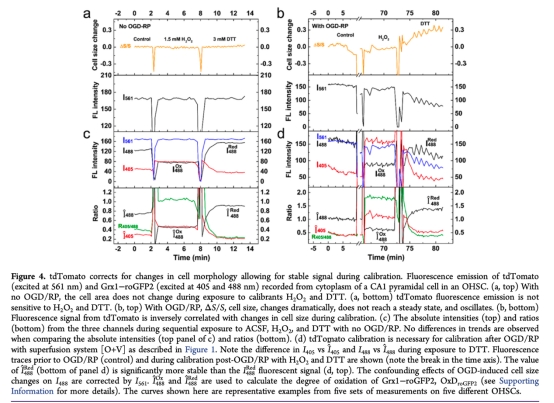
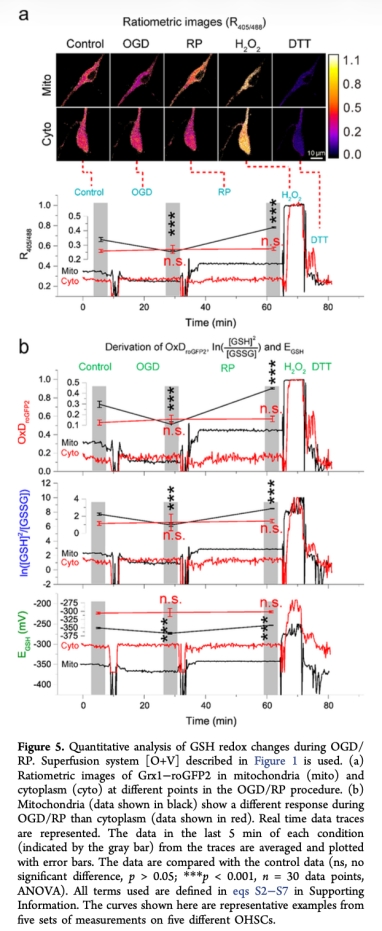
5. 測量了線粒體和細胞質中GSH氧化還原狀態在OGD/RP過程中的變化(圖5),研究意義是揭示了線粒體GSH系統在OGD期間更還原、RP期間更氧化的動態變化,而細胞質無顯著變化,表明線粒體對氧化應激更敏感,為理解腦卒中機制提供了新見解。
結論:
結論是線粒體GSH系統在OGD期間變得更還原(OxDroGFP2從0.30降至0.10),在RP期間變得更氧化(OxDroGFP2升至0.45),而細胞質中沒有顯著變化。這表明線粒體對氧化應激響應更敏感,可能由還原當量供應變化主導,而非ROS增加。該方法可用于藥理研究等擴展應用。
使用丹麥Unisense電極測量數據的研究意義:
使用丹麥Unisense電極測量pO2數據的研究意義在于,它優化了實驗的可靠性和可比性。通過測量pO2隨深度和時間的變化,研究驗證了優化灌注系統[O+V]能實現快速溶液交換(τ小于30秒),使pO2變化時間尺度(約2分鐘)與體內中風模型(如腦血流和pO2變化)一致。這確保了OGD/RP實驗條件更接近生理情況,提高了對GSH氧化還原狀態監測的準確性,為理解腦卒中中氧化應激機制提供了可靠工具。