熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Alteration of intracellular protein expressions as a key mechanism of the deterioration of bacterial denitrification caused by copper oxide nanoparticles
銅氧化物納米顆粒引起細菌反硝化惡化的關鍵機制:細胞內蛋白質表達的改變
來源:Scientific Reports, Volume 5, Article number 15824, 2015
《科學報告》,第5卷,文章編號15824,2015年
摘要
這篇論文摘要研究了銅氧化物納米顆粒(CuO NPs)對細菌反硝化作用的影響。研究發現,CuO NPs通過改變反硝化細菌Paracoccus denitrificans的關鍵蛋白質表達,顯著抑制反硝化過程。隨著CuO NPs濃度從0.05 mg/L增加到0.25 mg/L,總氮去除效率從98.3%降至62.1%。細胞形態和完整性分析表明納米顆粒進入細胞內部。蛋白質組學分析顯示,CuO NPs調控了氮代謝、電子傳遞和物質運輸相關蛋白質的表達。例如,負責葡萄糖轉運的GtsB蛋白下調導致NADH(反硝化電子供體)生成減少,同時電子傳遞蛋白(如NADH脫氫酶和細胞色素)表達受抑制,影響反硝化電子流。進一步實驗證實CuO NPs顯著降低硝酸還原酶和亞硝酸還原酶的活性和表達。這些結果從分子機制層面揭示了CuO NPs對細菌反硝化的負面影響。
研究目的
研究目的是探討CuO NPs對細菌反硝化過程的抑制機制,特別是從細胞內蛋白質表達改變的角度,以理解納米材料在環境中的生態風險,并為控制納米污染提供理論依據。
研究思路
研究思路基于使用模型反硝化細菌Paracoccus denitrificans,暴露于不同濃度CuO NPs(0-0.25 mg/L)下,通過多尺度方法分析反硝化性能變化。首先測量反硝化效率(硝酸鹽、亞硝酸鹽、N2O濃度),然后通過掃描電鏡(SEM)、透射電鏡(TEM)和乳酸脫氫酶(LDH)釋放評估細胞形態和完整性。利用iTRAQ蛋白質組學技術分析全蛋白表達變化,并通過生物信息學(GO、KEGG、STRING)分類差異蛋白功能。進一步使用多反應監測(MRM)定量關鍵蛋白表達,并測量酶活性和代謝物(如NADH、鐵攝取)以驗證機制。整體思路從宏觀性能到微觀分子機制,整合生理、蛋白組學和酶學分析。
測量的數據及研究意義
1 測量了反硝化性能參數,包括硝酸鹽(NO3--N)、亞硝酸鹽(NO2--N)和氧化亞氮(N2O-N)濃度變化,數據來自圖1。研究意義在于直接量化CuO NPs對反硝化過程的抑制程度,顯示濃度依賴性效率下降和中間產物積累,為納米毒性評估提供劑量效應基礎。
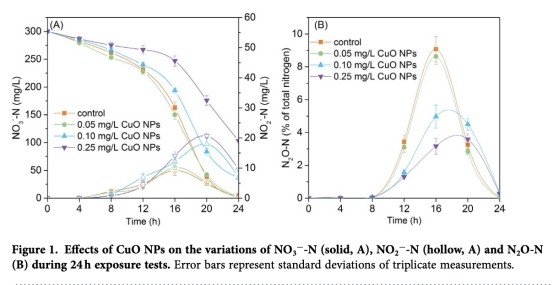
2 測量了細胞形態和完整性,通過SEM、TEM和LDH釋放實驗,數據來自圖2。研究意義在于證實CuO NPs吸附于細胞表面并進入胞內,導致膜損傷,闡明納米顆粒的物理侵入途徑是毒性起始點。
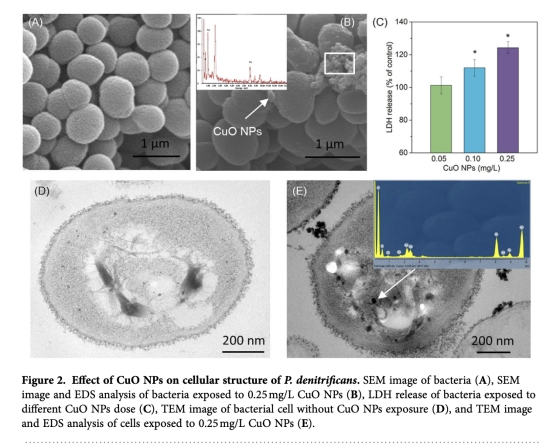
3 測量了全蛋白質組表達變化,通過iTRAQ技術識別138個差異表達蛋白,數據來自圖3。研究意義在于全局揭示CuO NPs調控的蛋白網絡,突出氮代謝、電子傳遞和轉運等關鍵通路,為機制假設提供組學證據。
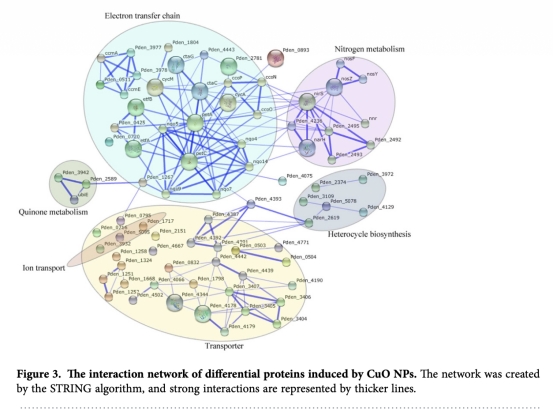
4 測量了葡萄糖轉運和NADH生成,顯示GtsB蛋白下調和葡萄糖利用減少,數據來自圖4A-B。研究意義在于鏈接物質轉運障礙與電子供體短缺,解釋反硝化能量供應受損的原因。
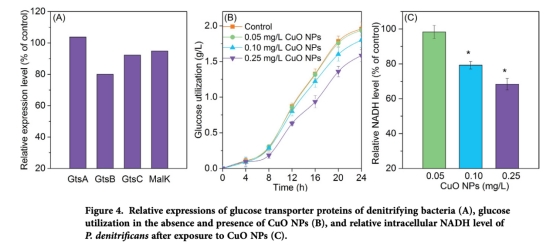
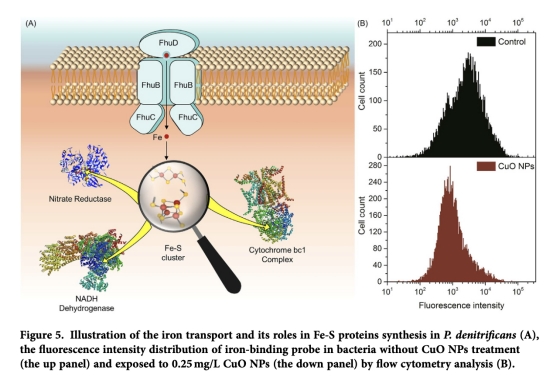
5 測量了鐵攝取和相關蛋白表達,通過熒光探針和流式細胞術,數據來自圖5。研究意義在于表明鐵轉運蛋白FhuD下調導致胞內鐵缺乏,影響鐵硫蛋白合成,從而破壞電子傳遞酶功能。
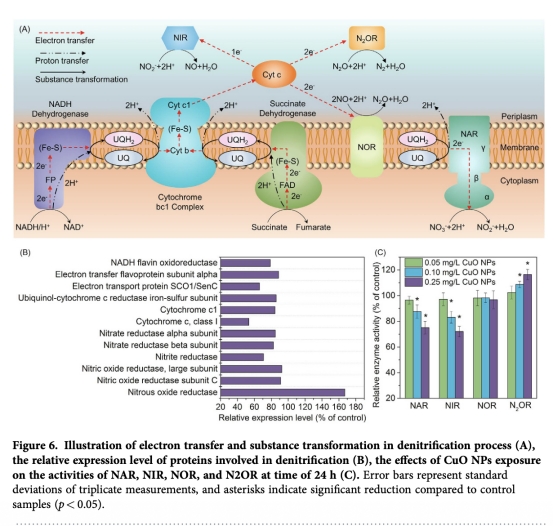
6 測量了電子傳遞蛋白和反硝化酶表達及活性,包括NADH脫氫酶、細胞色素和還原酶,數據來自圖6。研究意義在于直接驗證關鍵蛋白表達抑制與酶活性下降一致,從分子到功能層面完整闡述反硝化途徑受阻機制。
結論
1 CuO NPs以濃度依賴方式抑制反硝化性能,導致硝酸鹽去除率下降、亞硝酸鹽積累和N2O排放減少。
2 CuO NPs通過破壞細胞膜完整性進入胞內,引發全局蛋白質表達改變,關鍵涉及氮代謝、電子傳遞和物質轉運通路。
3 具體機制包括葡萄糖轉運蛋白下調減少NADH生成、鐵攝取障礙影響金屬酶合成、電子傳遞蛋白表達抑制削弱電子流,以及反硝化酶活性降低,共同導致反硝化功能惡化。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense電極測量的數據主要涉及溶解氧(DO)和反硝化酶活性(如NOR和N2OR)的定量。在溶解氧測量中,Unisense微電極用于監測流動細胞流出液的DO濃度,結果顯示CuO NPs暴露下DO從9.0 mg/L降至0.5 mg/L(補充數據相關部分),這一測量意義在于精確量化好氧代謝對微環境的影響,排除溶解銅離子干擾,證實CuO NPs通過物理化學作用而非離子釋放主導氧消耗。在酶活性測量中,Unisense微傳感器用于檢測一氧化氮還原酶(NOR)和氧化亞氮還原酶(N2OR)的催化活性(圖6C),數據結合蛋白表達驗證了CuO NPs對特定酶的抑制或促進(如N2OR上調)。這些高分辨率測量意義在于提供實時、動態的生理參數,將分子表達變化與功能輸出直接關聯,增強機制解釋的可靠性,并為環境納米毒性評估提供精準工具。