熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Cell inactivation by combined low dose-rate irradiation and intermittent hypoxia
聯合低劑量率輻射和間歇性缺氧對細胞的滅活作用
來源:International Journal of Radiation Biology, Volume 91, Issue 4 , 2015 , Pages 336-345
《國際放射生物學雜志》,第91卷第4期,2015年,第336-345頁
摘要:
這篇論文摘要討論了先前觀察到的聯合效應:低劑量率β-輻射(劑量率為15 mGy/h)與持續間歇性缺氧相結合,導致大約3-6周后出現大量細胞死亡。研究通過將[3H]標記的纈氨酸摻入細胞蛋白來實現連續低劑量率β-輻射,并在缺氧手套箱中培養細胞。在整個實驗過程中監測了克隆形成能力、細胞周期分布和細胞呼吸。結果表明,聯合處理后大多數細胞死亡,存活率僅為1-2%,但繼續培養后少數存活細胞在氧氣供應增加時重新開始增殖。在比15 mGy/h低10倍和25倍的劑量率下輻射T-47D細胞,對克隆形成能力沒有顯著影響。結論是低劑量率β-輻射對間歇性缺氧細胞有特異性滅活作用,超過98%的細胞被滅活,但在氧氣條件改善后少數存活細胞能重啟增殖。
研究目的:
研究目的是詳細調查低劑量率輻射(劑量率為15 mGy/h)與持續間歇性缺氧聯合導致大量細胞死亡的機制。研究旨在通過監測克隆形成能力、細胞周期分布和細胞呼吸等參數,探討這種聯合處理對T-47D乳腺癌細胞的影響,并確定劑量率和氧氣條件在細胞滅活中的作用,為理解腫瘤中缺氧細胞的輻射響應提供新見解。
研究思路:
研究思路基于使用[3H]標記的纈氨酸摻入細胞蛋白實現連續低劑量率β-輻射(劑量率為15、1.5或0.6 mGy/h),并在缺氧手套箱中控制氧氣濃度(4% O2)模擬間歇性缺氧條件。通過克隆形成實驗定量細胞存活率,使用流式細胞術分析細胞周期分布,并通過丹麥Unisense微電極系統測量細胞周圍氧氣濃度和細胞呼吸速率。研究比較了不同劑量率輻射下細胞的響應,并分析了[3H]-纈氨酸攝取以排除劑量差異的影響。整體思路結合輻射生物學和微環境監測,從細胞存活、生理變化和氧氣動態多角度探討聯合處理的效應。
測量的數據及研究意義:
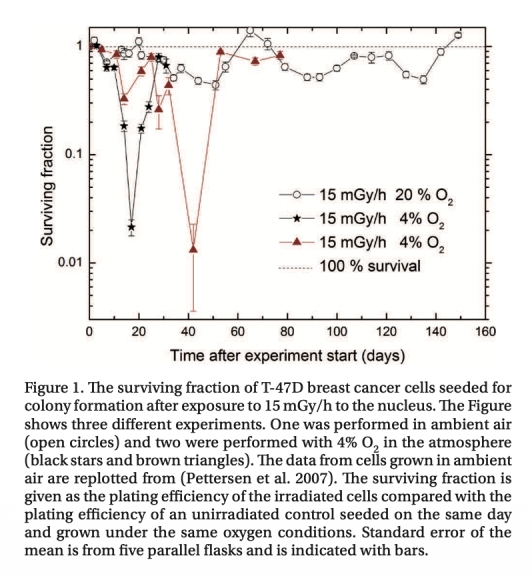
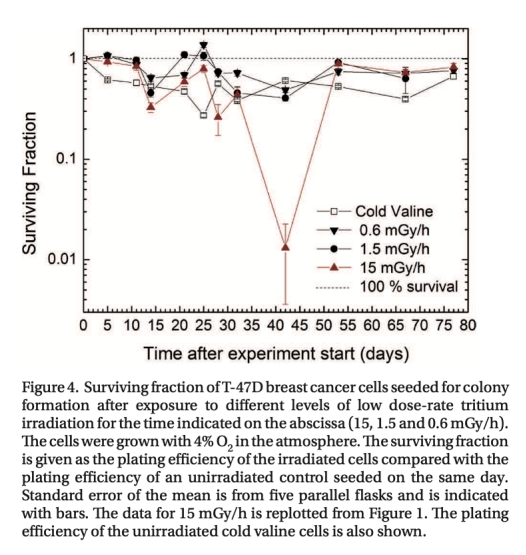
1 測量了細胞存活率(克隆形成能力),數據來自圖1、圖2、圖4和圖6E。研究意義在于顯示15 mGy/h輻射與間歇性缺氧聯合導致存活率急劇下降至1-2%,而較低劑量率(1.5和0.6 mGy/h)或單獨處理影響較小,表明聯合處理對缺氧細胞有特異性滅活作用,為靶向腫瘤缺氧區域提供了新策略。
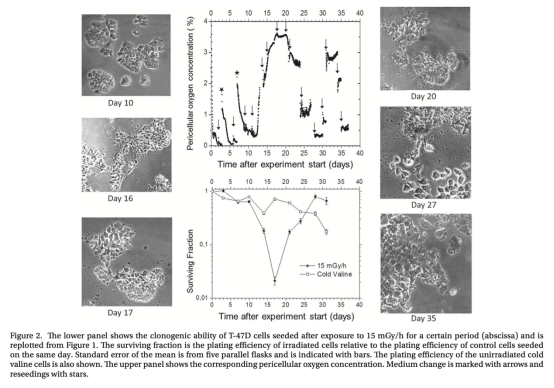
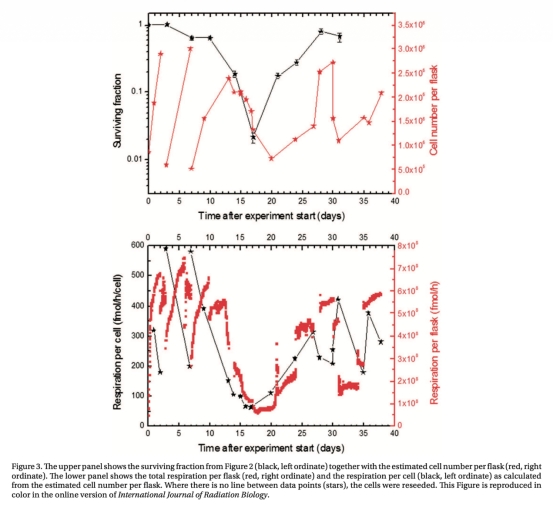
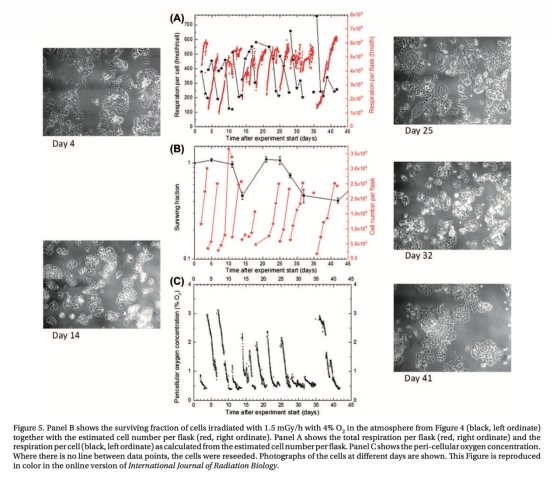
2 測量了細胞周圍氧氣濃度和細胞呼吸速率,使用丹麥Unisense微電極,數據來自圖2、圖3和圖5。研究意義在于揭示輻射細胞呼吸速率升高(達600 fmol/細胞/小時),導致氧氣耗盡和極端缺氧,從而引發細胞死亡;氧氣動態數據直接關聯了呼吸變化與存活率下降,明確了微環境在輻射響應中的關鍵作用。
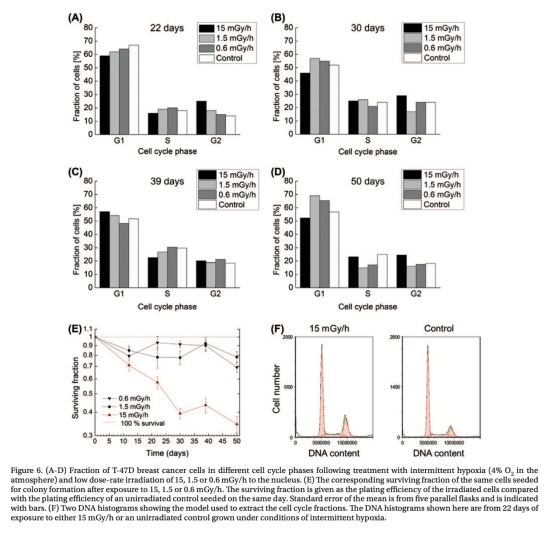
3 測量了細胞周期分布,數據來自圖6A-D。研究意義在于顯示聯合處理引起G2期積累趨勢,但未顯著改變周期分布,表明細胞死亡主要非周期阻滯驅動,而是與代謝應激相關,補充了輻射誘導死亡的機制理解。
4 測量了[3H]-纈氨酸攝取。研究意義在于排除缺氧細胞輻射劑量增加的可能性,確認效應源于生理響應而非劑量差異,強化了聯合處理的生物學特異性。
結論:
研究得出結論,低劑量率輻射(15 mGy/h)與間歇性缺氧聯合對T-47D細胞有協同滅活效應,導致超過98%細胞死亡,但少數存活細胞在氧氣改善后可恢復增殖。這種效應非劑量依賴,而是由輻射誘導的呼吸速率升高加劇缺氧所驅動,表明其機制不同于傳統輻射響應,可能用于靶向腫瘤缺氧細胞。
使用丹麥Unisense電極測量數據的研究意義:
使用丹麥Unisense微電極測量的氧氣濃度和呼吸數據(來自圖2、圖3和圖5)具有關鍵研究意義。這些測量直接量化了細胞微環境動態:顯示輻射細胞呼吸速率升至600 fmol/細胞/小時(遠高于未輻射細胞),導致氧氣濃度從4%降至低于0.1%,引發極端缺氧。意義在于首次將輻射響應與實時氧氣消耗關聯,證實呼吸加劇是聯合處理中細胞死亡的核心驅動力——缺氧非單純環境條件,而是輻射誘導的代謝應激后果。這顛覆了傳統氧效應(缺氧通常保護細胞),揭示了低劑量率輻射對缺氧細胞的特異性,為腫瘤治療中利用微環境提供了新視角。此外,數據還顯示存活細胞在氧氣供應恢復后增殖,強調了微環境可逆性的重要性,指導了聯合治療時機優化。