熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Denitrification by cystic fibrosis pathogens–Stenotrophomonas maltophilia is dormant in sputum
囊性纖維化病原體的反硝化作用 - 嗜麥芽窄食單胞菌在痰液中處于休眠狀態
來源:International Journal of Medical Microbiology xxx (2014)
論文摘要
本研究探討了四種囊性纖維化(CF)肺部感染病原體——銅綠假單胞菌(Pseudomonas aeruginosa)、木糖氧化無色桿菌(Achromobacter xylosoxidans)、多噬伯克霍爾德菌(Burkholderia multivorans)和嗜麥芽窄食單胞菌(Stenotrophomonas maltophilia)在厭氧條件下的反硝化能力及其與病原性的關系。通過厭氧培養實驗和微傳感器技術,研究發現高病原性菌株(P. aeruginosa、A. xylosoxidans、B. multivorans)能利用硝酸鹽(NO??)或亞硝酸鹽(NO??)進行反硝化,并產生氧化亞氮(N?O),而低病原性菌株S. maltophilia幾乎無N?O生成且生長受限。在CF患者痰液中,S. maltophilia的核糖體含量低,表明其處于休眠狀態。結果表明,反硝化能力可能增強病原體在缺氧環境(如CF痰液)中的存活和致病性,而S. maltophilia因缺乏完整反硝化途徑導致低病原性。
研究目的
本研究旨在:
比較不同CF病原體(高病原性與低病原性)在厭氧條件下的反硝化活性,特別是N?O的產生能力。
評估反硝化作用對病原體厭氧生長的貢獻,及其與臨床病原性的關聯。
探究S. maltophilia在CF痰液中的代謝狀態(如休眠),以解釋其較低致病性。
驗證反硝化作為CF肺部感染中細菌存活的潛在機制。
研究思路
研究采用多方法結合的實驗策略:
菌株分離與培養:從32名慢性感染患者分離病原體菌株(P. aeruginosa 12株、A. xylosoxidans 9株、B. multivorans 9株、S. maltophilia 7株),在厭氧LB培養基中培養,添加NO??或NO??(10 mM)作為電子受體。
反硝化活性測量:使用丹麥Unisense N?O微傳感器(N?O-100型,尖端直徑100 μm)實時測量培養物中的N?O濃度,量化反硝化速率。
生長與代謝分析:
通過光密度(OD600)和菌落計數(CFU/mL)評估生物量積累。
使用Griess法測量NO??和NO??的消耗。
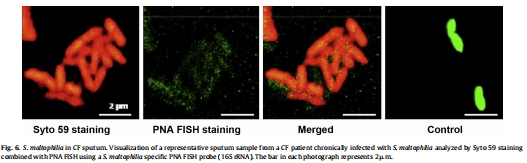
痰液樣本分析:對CF患者痰液進行PNA FISH(肽核酸熒光原位雜交)染色,檢測S. maltophilia的16S rRNA含量,推斷其生長速率。
統計驗證:采用ANOVA和Dunnett檢驗進行組間比較,確保結果顯著性(p ≤ 0.05)。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
N?O產生數據:
數據內容:在厭氧培養中,P. aeruginosa、A. xylosoxidans和B. multivorans在添加NO??后N?O濃度顯著升高(如P. aeruginosa在2天后N?O峰值),而S. maltophilia無顯著N?O生成。添加NO??時,僅P. aeruginosa有N?O積累。
研究意義:直接證明高病原性菌株具有反硝化能力,而S. maltophilia缺乏該功能,反硝化完整性可能與病原性正相關。數據來自(圖示N?O濃度隨時間變化)。
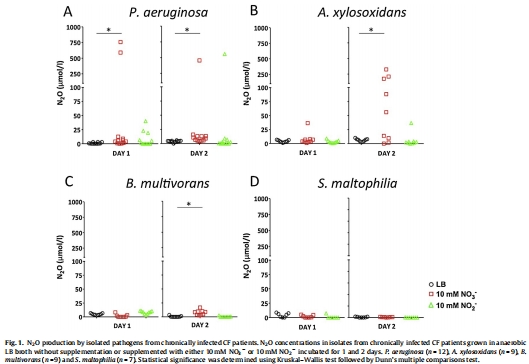
生物量積累數據:
數據內容:所有菌株在添加NO??后OD600增加,但S. maltophilia增長最慢(2天后OD600僅為其他菌株的50%);添加NO??僅促進P. aeruginosa生長。
研究意義:表明NO??還原支持厭氧生長,但S. maltophilia效率低,提示其代謝缺陷。數據來自(生物量對比)。
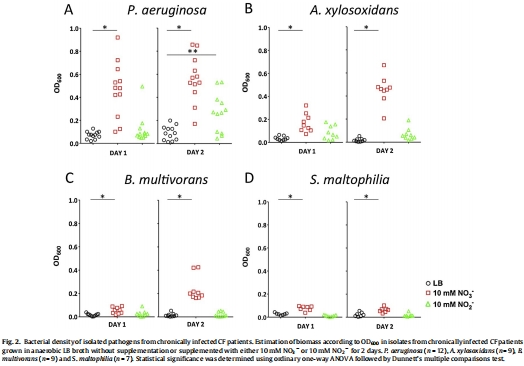
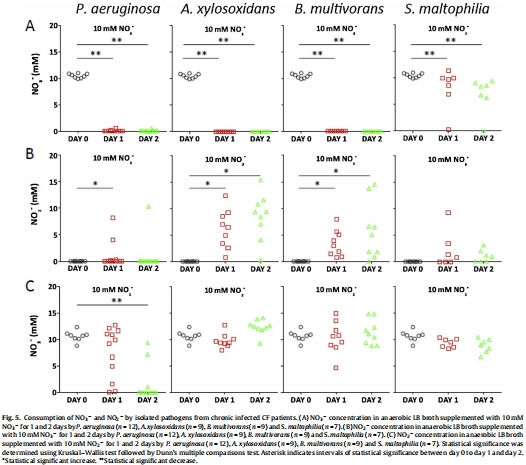
NO??和NO??消耗數據:
數據內容:所有菌株均消耗NO??,但僅P. aeruginosa能完全去除NO??;S. maltophilia的NO??消耗不完全,且無NO??積累。
研究意義:證實P. aeruginosa有完整反硝化途徑(至N?O),而S. maltophilia可能僅進行硝酸鹽還原(至NO??),無法進一步反硝化。數據來自(離子濃度變化)。

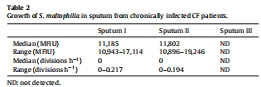
痰液中細菌生長狀態數據:
數據內容:PNA FISH顯示S. maltophilia在痰液中核糖體含量低,特定生長率中位數為0 divisions/h(范圍0–0.217),表明休眠。
研究意義:結合厭氧實驗,說明S. maltophilia在CF缺氧環境中代謝不活躍,解釋其低病原性。數據來自文本中“Growth of isolates”部分和Table 2(生長率統計)。

視覺生長檢查數據:
數據內容:厭氧培養2天后,P. aeruginosa和A. xylosoxidans在添加NO??時形成明顯渾濁,S. maltophilia生長微弱。
研究意義:直觀驗證反硝化對生長的促進作用。數據來自(培養物照片)。
研究結論
高病原性CF菌株(P. aeruginosa、A. xylosoxidans、B. multivorans)能通過反硝化(產生N?O)在厭氧環境中生長,這可能增強其在CF痰液缺氧條件下的存活和致病性。
S. maltophilia反硝化能力缺失(無N?O生成)且厭氧生長受限,在痰液中處于休眠狀態,這與其較低臨床病原性一致。
反硝化完整性(如NO??還原至N?O)可能是CF病原體適應缺氧微環境的關鍵 virulence 因子。
研究為CF感染管理提供新見解:針對反硝化途徑可能有助于控制高病原性菌株的持續感染。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense N?O微傳感器測量的N?O數據具有關鍵研究意義,其詳細解讀如下:
高精度實時監測反硝化活性:Unisense N?O微傳感器是一種電化學傳感器,具備高靈敏度(檢測限達納摩爾級)和快速響應能力(秒級)。本研究將其用于厭氧培養系統,直接實時測量了病原體在添加NO??或NO??后產生的N?O濃度動態變化(如Fig.1所示)。這種原位連續監測避免了傳統終端取樣的誤差,能準確捕捉反硝化過程的啟停動態,例如P. aeruginosa在24小時內N?O的快速上升,為“反硝化活躍”提供了最直接的證據。
量化病原體代謝差異:傳感器數據顯示,高病原性菌株的N?O產率顯著高于S. maltophilia(后者幾乎無信號),將抽象的“反硝化能力”轉化為可量化的指標。例如,P. aeruginosa的N?O積累曲線(Fig.1)與其厭氧生長數據(Fig.2)吻合,強有力地證明反硝化能量代謝支持細菌增殖,而S. maltophilia的缺失數據解釋其休眠狀態。
驗證反硝化與病原性的關聯:N?O是反硝化途徑的特異性中間產物,其檢測確認了高病原性菌株擁有完整的反硝化酶系(如硝酸鹽還原酶和亞硝酸鹽還原酶)。Unisense數據將代謝表型(反硝化)與臨床觀察(病原性)直接鏈接,支持了“反硝化增強CF病原體適應性”的假說。
方法學優勢:Unisense傳感器通過線性校準(用N?O飽和PBS)確保數據準確性,其微創設計(尖端100 μm)避免擾動培養系統。本研究通過重復剖面測量(6次重復),提供了統計可靠的數據,為結論奠定技術基礎。
總之,丹麥Unisense電極的數據不僅是本研究中驗證反硝化活性的核心技術證據,更通過提供高精度N?O動力學曲線,揭示了病原體代謝多樣性如何影響其在CF缺氧環境中的生存策略,凸顯了微傳感器在微生物致病機制研究中的不可替代價值。