熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Changes in Glucose Fermentation Pathways by an Enriched Bacterial Culture in Response to Regulated Dissolved H2 Concentrations
富集細菌培養物響應調節的溶解 H2濃度而改變葡萄糖發酵途徑
來源:Biotechnol. Bioeng. 2015;112: 1177–1186.
論文摘要
本研究通過開發一種灌注系統(結合膜過濾和氣體噴射),在連續葡萄糖發酵過程中控制溶解氫氣(H2)濃度,以探究富集細菌培養物(主要含Thermoanaerobacterium thermosaccharolyticum)的發酵途徑變化。研究發現,通過調節葡萄糖進料速率(0.5–2 g/d)和噴射條件,溶解H2濃度可低至3 kPa(以平衡分壓計)。在低H2濃度下,H2產量顯著提高(最高達2.67 mol H2/mol葡萄糖,比無噴射條件高300%),發酵產物從還原性產物(如丁酸、乙醇)轉向氧化性產物(如乙酸)。研究還使用H2調節分配模型模擬產品形成趨勢,模型在低H2濃度下預測準確,但在高H2濃度下高估乙酸產量。結果表明,直接測量溶解H2濃度對理解發酵途徑調控至關重要。
研究目的
本研究旨在:
開發一種灌注系統,實現對連續發酵過程中溶解H2濃度的精確控制。
評估不同溶解H2濃度下細菌培養物的葡萄糖發酵途徑變化,特別是H2產量和產物分布。
比較實驗觀測的H2產量與基于H2調節分配模型(如Mosey模型)的預測結果。
驗證溶解H2濃度在調節發酵途徑中的熱力學作用,并揭示H2超飽和現象的影響。
研究思路
研究采用實驗與模型模擬相結合的方法:
系統設計:構建灌注系統,包括連續攪拌槽反應器(CSTR)、燒結金屬膜過濾器(用于保留生物質)和噴射罐(用于去除溶解H2)。系統允許在無細胞剪切條件下劇烈噴射培養基。
實驗操作:在60°C下運行反應器,水力停留時間(HRT)為36小時。通過改變葡萄糖進料速率(2 g/d、1 g/d、0.5 g/d)和噴射條件,實現不同溶解H2濃度的穩態發酵。
溶解H2測量:使用丹麥Unisense H2微傳感器(H2-500) 實時測量反應器和噴射罐上下游的溶解H2濃度,傳感器每日校準三次,確保數據準確性。
樣品分析:
氣體分析:通過氣相色譜(GC)測量頭部空間的H2、CO2和CH4濃度。
液體分析:通過高效液相色譜(HPLC)測量葡萄糖、甲酸、琥珀酸和乳酸濃度;通過氣相色譜-火焰離子化檢測器(GC-FID)測量揮發性脂肪酸(VFA)和酒精濃度。
生物質濃度:采用標準方法每日測量。
模型模擬:應用Mosey(1983)的H2調節分配模型,基于溶解H2濃度和pH預測發酵產物分布(如乙酸、丁酸、乙醇、丁醇的生成速率)。
數據比較:將實驗測量的產物形成速率與模型預測值對比,評估模型準確性。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
溶解H2濃度數據:
數據內容:在不同葡萄糖進料速率下,溶解H2濃度(以平衡分壓表示)從50–54%(無噴射)降至3%(0.5 g/d進料)。數據顯示H2超飽和現象,例如在0.5 g/d時,溶解H2濃度是頭部空間分壓的7倍。
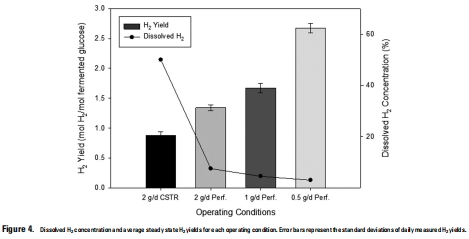
研究意義:直接證明灌注系統能有效降低溶解H2濃度,并揭示H2超飽和對發酵熱力學的關鍵影響,挑戰了僅憑頭部空間測量推斷溶解濃度的傳統方法。數據來自圖3(頂部面板,顯示溶解H2濃度隨時間變化)和圖4(溶解H2濃度與H2產量關系)。
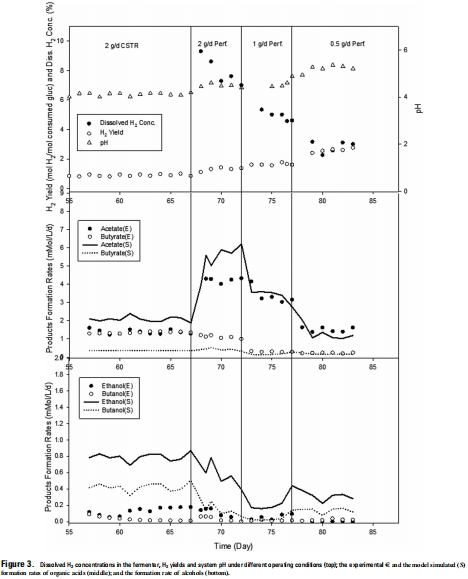
H2產量和產物形成速率數據:
數據內容:H2產量隨溶解H2濃度降低而增加,從0.88 mol H2/mol葡萄糖(無噴射)升至2.67 mol H2/mol葡萄糖(0.5 g/d)。乙酸產量增加300%,而丁酸和乙醇產量下降34–46%。
研究意義:驗證了低H2濃度促進氧化途徑(如乙酸生成)的理論,為通過H2控制優化發酵產氫提供實驗依據。數據來自圖3(中部和底部面板,顯示有機酸和酒精形成速率)和圖4(H2產量與溶解H2濃度關系)。
模型模擬與實驗對比數據:
數據內容:模型在低H2濃度(<6 kPa)下準確預測乙酸和H2產量,但在高H2濃度下高估乙酸產量,低估丁酸產量。模型預測丁酸產量峰值僅為0.15 mol/mol葡萄糖,而實驗值達0.55 mol/mol。
研究意義:表明模型能捕捉趨勢,但需改進以解釋細菌偏好(如Thermoanaerobacterium在高H2下傾向產丁酸)。數據來自圖3(模擬與實驗值對比)和圖5(模型預測的產品產量隨H2濃度變化曲線)。
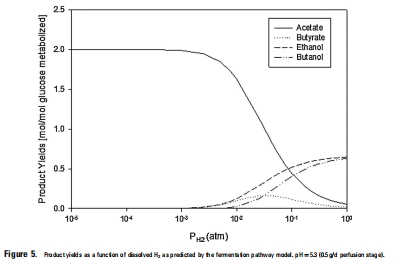
葡萄糖消耗和系統pH數據:
數據內容:葡萄糖消耗率隨H2濃度降低而增加,在0.5 g/d時殘余葡萄糖降至0.001 g/L;系統pH穩定在5.3左右。
研究意義:證實低H2濃度提升發酵效率,pH穩定性排除了酸堿干擾。數據集成在圖3中。
研究結論
灌注系統能有效控制溶解H2濃度,最低可至3 kPa,為研究H2調節發酵提供了可靠平臺。
低溶解H2濃度顯著提高H2產量(最高2.67 mol/mol葡萄糖)和乙酸產量,同時抑制還原性產物(如丁酸、乙醇)生成,表明發酵途徑向氧化方向偏移。
H2調節分配模型在低H2濃度下預測良好,但在高H2濃度下存在偏差,提示需結合菌株特異性代謝偏好改進模型。
溶解H2超飽和現象普遍存在,強調直接測量溶解濃度(而非依賴頭部空間)的必要性,以避免熱力學誤解。
研究為優化生物產氫過程提供了實踐指導,通過控制H2濃度可調控產物分布,提升能源回收效率。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense H2微傳感器測量的溶解H2數據具有關鍵研究意義,其詳細解讀如下:
高精度實時監測溶解H2濃度:Unisense H2微傳感器是一種電化學傳感器,具備高靈敏度(檢測限低)和快速響應能力。本研究將其集成于在線密封腔室中,實時測量反應器和噴射罐上下游的溶解H2濃度,每日通過三點校準(0.005%、3%、21% H2)確保數據準確性。這種直接原位測量避免了傳統方法依賴頭部空間平衡的假設,首次在連續發酵中量化了溶解H2的動態變化,為熱力學分析提供了可靠輸入。
揭示H2超飽和現象及其熱力學影響:數據顯示,溶解H2濃度始終高于頭部空間平衡值(超飽和因子達7倍),證明發酵系統中H2傳質限制普遍存在。這種超飽和現象解釋了為何簡單頭部空間測量會低估溶解濃度,進而誤導熱力學計算。Unisense數據直接將H2超飽和與發酵途徑變化關聯,例如在低進料速率下,高超飽和反而加劇了H2積累抑制,凸顯了實時監測對過程優化的重要性。
支撐模型驗證與機制闡釋:Unisense測量的溶解H2濃度是H2調節分配模型的核心輸入參數。通過比較模型預測與實驗數據(圖3),驗證了溶解H2濃度作為發酵途徑主控因子的角色。例如,低H2濃度下模型準確性高,證實了熱力學平衡主導途徑選擇;而高H2下的偏差提示需考慮動力學或菌株特異性因素。
方法學優勢與可靠性:Unisense傳感器的微創設計和在線校準消除了取樣擾動,其高時間分辨率能捕捉H2濃度的瞬時波動(如進料變化后的響應)。本研究通過同步測量噴射罐上下游濃度,量化了H2去除效率,為灌注系統優化提供了直接依據。
總之,丹麥Unisense電極的數據不僅是本研究中量化H2濃度的技術基石,更通過提供高精度溶解H2證據,揭示了超飽和現象和熱力學調控機制,推動了發酵產氫研究從黑箱向定量化發展。