熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Changes in bacterial community metabolism and composition during the degradation of dissolved organic matter from the jellyfish Aurelia aurita in a Mediterranean coastal lagoon
地中海水母Aurelia aurita 溶解有機物降解過程中細菌群落代謝和組成的變化
來源:Sorbonne Universités,
論文摘要
本研究探討了地中海沿海瀉湖(Bages-Sigean Lagoon)中細菌群落對水母Aurelia aurita溶解有機物(DOM)添加的響應。通過22天的微宇宙實驗,研究發現水母DOM高度可生物降解,添加后導致溶解有機碳(DOC)和氮(DON)快速礦化,并引起銨(NH??)和正磷酸鹽(PO?3?)積累。細菌代謝在DOM添加初期(前2天)顯著增強,異養原核生物生產量(HPP)和呼吸速率(HPR)迅速上升,但細菌生長效率(BGE)始終低于20%,表明DOM主要通過呼吸消耗而非生物量生產。細菌群落結構發生顯著變化:初期以Pseudoalteromonas和Vibrio(Gammaproteobacteria)為主,中期轉為Bacteroidetes優勢,后期Alphaproteobacteria比例增加。細菌代謝功能(如生產量和呼吸)在實驗末期恢復至對照水平,但群落多樣性未完全恢復,表明水母水華可能對沿海瀉湖細菌群落結構產生持久影響。
研究目的
本研究旨在:
評估水母Aurelia aurita的DOM對沿海瀉湖細菌群落代謝(如生產量、呼吸)和組成(多樣性)的短期與長期影響。
量化DOM降解過程中營養鹽(如DOC、DON、DOP、無機氮磷)的動態變化,揭示DOM的生物可利用性。
分析細菌群落的演替模式,識別響應DOM添加的關鍵類群。
探究細菌群落在DOM擾動后的恢復力(resilience),比較代謝功能與多樣性恢復的差異。
為水母水華對海洋碳循環和生態系統功能的潛在影響提供實驗證據。
研究思路
研究采用微宇宙實驗與多參數測量相結合的系統方法:
實驗設計:從地中海瀉湖采集海水,過濾去除大顆粒后,設置對照組(僅瀉湖水)和DOM添加組(添加水母A. aurita提取的DOM)。每組3個重復,在黑暗、18°C下培養22天,定期采樣(T0、T2、T9、T22)。
理化參數測量:監測營養鹽(NO??+NO??、NH??、PO?3?)、DOC、DON、DOP濃度,以及有色DOM(CDOM)的熒光特性(蛋白質樣和腐殖樣組分)。
生物參數測量:
病毒豐度:通過流式細胞術計數。
細菌豐度、生產量(HPP,使用3H-胸苷摻入法)和呼吸速率(HPR,使用丹麥Unisense氧微電極測量)。
細菌生長效率(BGE)計算:BGE = HPP / (HPP + HPR)。
群落結構分析:
可培養細菌分離與鑒定:通過平板培養和16S rRNA基因測序。
分子生物學方法:CE-SSCP指紋圖譜和16S rRNA基因焦磷酸測序(bTEFAP)分析細菌多樣性。
數據分析:使用統計方法(如ANOVA、Bray-Curtis相似性、CCA)評估處理間差異和環境影響因子。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
營養鹽和DOM濃度數據:
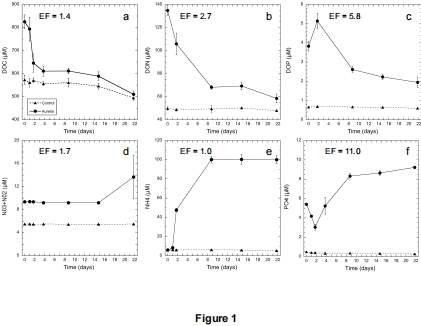
數據內容:DOM添加組中DOC在前期(0-4天)快速消耗(速率57 μM d?1),后期減緩;DON在T9前下降67 μM;NH??濃度在T9升至100 μM,PO?3?先降后升。對照組長變化緩慢。
研究意義:表明水母DOM高度可降解,并釋放無機營養鹽,可能刺激初級生產或導致富營養化。數據來自圖1a-f(營養鹽時序變化)。
CDOM熒光數據:
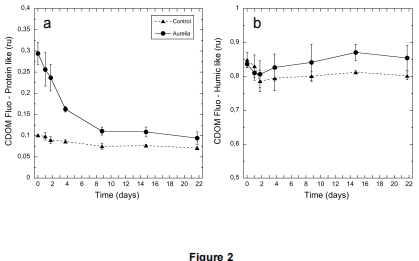
數據內容:DOM添加組的蛋白質樣熒光(275/340 nm)在T9前快速下降,腐殖樣熒光(320/420 nm)在后期略升。
研究意義:反映DOM組成從易降解蛋白向難降解腐殖質轉化,提示降解過程的化學演化。數據來自圖2a-b(CDOM熒光曲線)。
病毒和細菌豐度數據:
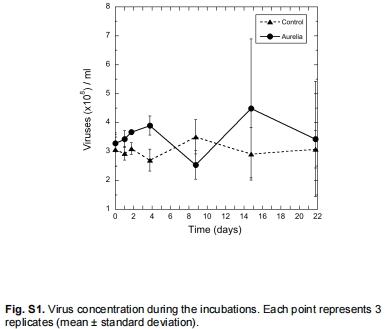
數據內容:病毒豐度在兩組間無顯著差異,但DOM組在T2、T4略高。細菌豐度在DOM組T3達峰值后驟降94%(T4),對照組長穩定。
研究意義:病毒可能不是細菌下降主因;細菌快速生長后崩潰,暗示資源耗盡或捕食。數據來自圖S1(病毒豐度)和圖3a(細菌豐度)。
細菌代謝數據(生產量、呼吸、BGE):
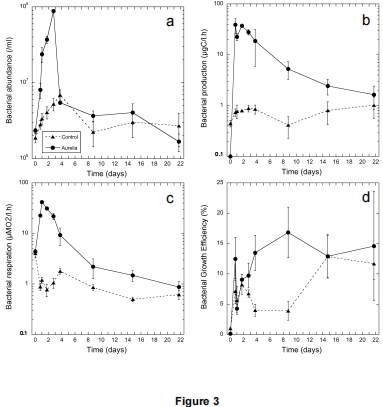
數據內容:DOM組HPP和HPR在T2達峰值(如HPP升高),后逐漸下降;BGE初始<1%,T9升至17%,始終低于20%。
研究意義:證實DOM主要通過呼吸礦化,碳流失嚴重;BGE低可能與能隙代謝有關。數據來自圖3b-d(HPP、HPR、BGE曲線)。
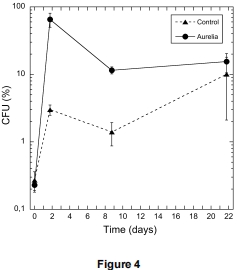
可培養細菌數據:
數據內容:DOM組可培養比例在T2達65%(對照僅3%),優勢菌從Gammaproteobacteria(如Pseudoalteromonas)轉向Bacteroidetes和Alphaproteobacteria。
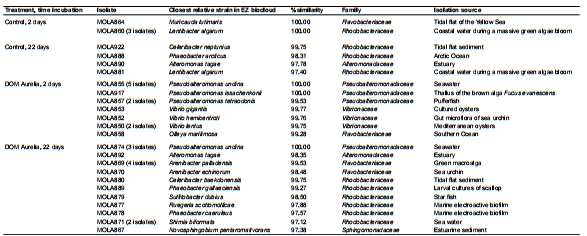
研究意義:顯示可培養部分對DOM的快速響應,且群落演替與分子數據一致。數據來自圖4(可培養比例)和表1(菌株鑒定)。

細菌群落結構數據:
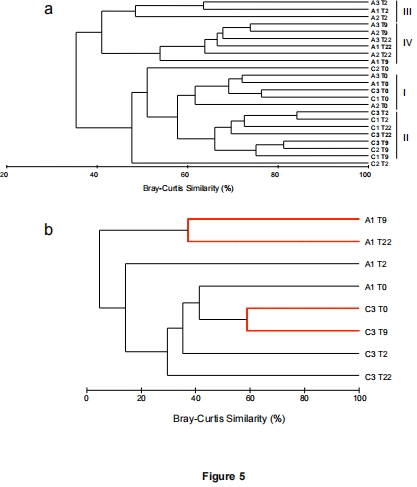
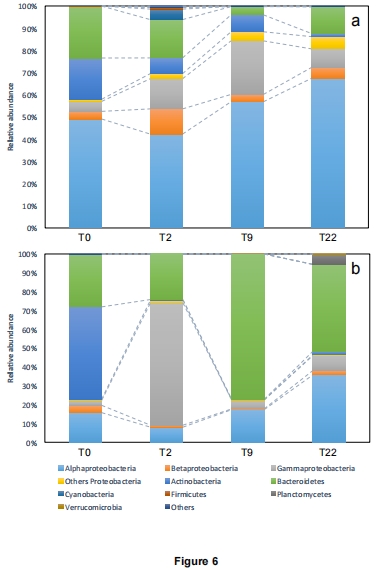
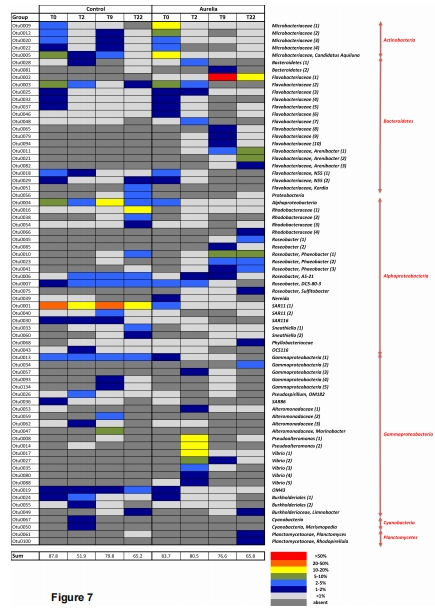
數據內容:CE-SSCP和焦磷酸測序顯示DOM組群落顯著偏離對照,T2時Gammaproteobacteria(OTU0008、0014)占65%,T9時Bacteroidetes(如Flavobacteriaceae)達77%,T22時Alphaproteobacteria(如Roseobacter)上升至36%。
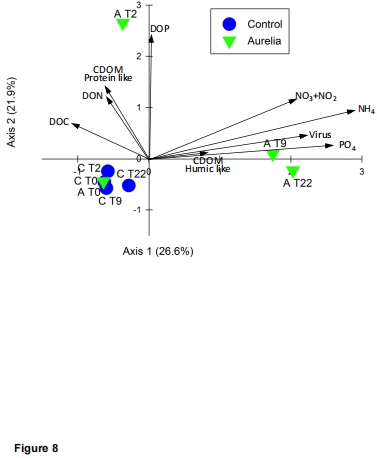
研究意義:揭示DOM驅動群落演替,不同類群在降解階段分工。數據來自圖5(聚類樹)、圖6(門水平組成)、圖7(OTU熱圖)和圖8(CCA分析)。
使用丹麥Unisense電極測量的呼吸數據:
數據內容:通過Unisense氧微電極測量微室中溶解氧消耗,計算HPR。數據顯示DOM組HPR在T2最高,后遞減。
研究意義:提供準確的呼吸速率,為BGE計算提供關鍵輸入。數據集成在圖3c的HPR曲線中。
研究結論
水母DOM是高度易降解的有機碳源,能快速刺激細菌代謝,但主要通向呼吸(BGE<20%),導致CO?釋放而非生物量積累。
細菌群落對DOM添加響應迅速且持久:先由機會主義者(Gammaproteobacteria)利用易降解組分,后由專化類群(Bacteroidetes)降解高分子物質,最后Alphaproteobacteria可能參與殘余物轉化。
群落代謝功能(生產量、呼吸)在22天內恢復至對照水平,但群落結構未完全恢復,表明功能冗余但多樣性變化持久。
水母水華可能通過釋放DOM改變沿海瀉湖的碳循環路徑,并引發細菌群落結構的長期偏移,對生態系統穩定性構成風險。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense氧微電極測量的細菌呼吸速率(HPR)數據具有關鍵研究意義,其詳細解讀如下:
高精度實時監測代謝活性:Unisense氧微電極是一種電化學傳感器,具有高靈敏度(精度0.05%)和快響應時間(<1秒),能實時測量微室中溶解氧的消耗速率。本研究將其用于直接量化異養原核生物的呼吸速率(HPR),通過線性回歸計算單位時間內的氧變化(方法部分描述)。這種原位測量避免了傳統 Winkler 滴定法的破壞性取樣誤差,提供了連續、動態的呼吸數據。
準確計算細菌生長效率(BGE)的核心依據:HPR數據與細菌生產量(HPP)結合,是計算BGE(BGE = HPP / (HPP + HPR))的基石。本研究顯示BGE始終低于20%(圖3d),直接證明水母DOM降解以呼吸為主導,碳大多礦化為CO?而非轉化為生物量。Unisense的精確測量確保了BGE結果的可靠性,為評估碳循環效率提供了定量證據。
揭示代謝動態與DOM降解的耦合關系:HPR在DOM添加后迅速升高(T2峰值),隨后下降(圖3c),反映了細菌對易降解DOM的快速響應和耗盡過程。這種時間分辨數據將呼吸動態與DOM消耗(圖1a)關聯,支持了“脈沖式資源輸入導致代謝爆發”的生態模型。
方法學優勢:Unisense電極的低氧消耗設計(外護陰極)和微室適配性使其適用于長期培養實驗。數據與其它參數(如營養鹽、豐度)同步采集,增強了多變量分析(如CCA,圖8)的說服力,幫助識別呼吸作用與環境因子的聯系。
總之,丹麥Unisense電極的數據不僅是本研究中量化代謝通量的技術基礎,更通過提供高精度呼吸速率,揭示了水母DOM降解的能量分配模式,凸顯了微傳感器在微生物生態代謝研究中的不可替代價值。