熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Silicification-Induced Cell Aggregation for the Sustainable Production of H2 under Aerobic Conditions
有氧條件下氫氣可持續生產的硅化作用誘導的細胞聚集
來源:Angew. Chem. Int. Ed. 2015, 54, 11961–11965
論文摘要
本文報道了一種通過硅化作用誘導綠藻(Chlorella pyrenoidosa)細胞聚集的方法,實現在自然有氧條件下可持續的光生物產氫。通常,綠藻的氫酶對氧氣高度敏感,無法在有氧環境中產氫。但研究發現,硅化處理形成的細胞聚集體具有核殼結構:表層細胞暴露于氧氣,而核心細胞處于缺氧微環境,從而激活氫酶并驅動產氫。這種結構平衡了光合作用電子生成與氫酶活性,使聚集體在連續光照下可持續產生氫氣,為太陽能驅動水分解制氫提供了新途徑。
研究目的
本研究旨在:
開發一種生物啟發式硅化方法,誘導綠藻細胞聚集,創造有氧條件下的缺氧微環境。
驗證聚集體能否在自然大氣環境中實現可持續光生物產氫。
探究聚集體的核殼結構如何通過空間功能分化(SFD)調節氧氣和氫氣分布。
評估聚集體尺寸對產氫效率的影響,優化系統性能。
研究思路
研究采用多學科實驗方法:
細胞聚集誘導:使用聚二烯丙基二甲基氯化銨(PDADMAC)模擬硅化蛋白,在Chlorella pyrenoidosa細胞表面誘導二氧化硅沉積,形成尺寸可控(10–500 μm)的聚集體。
產氫定性驗證:以三氧化鎢(WO?)粉末為指示劑(遇H?變藍色),直觀比較天然細胞與聚集體在光照下的產氫能力。
定量氣體分析:通過氣相色譜(GC)測量密閉玻璃管頂空中的氫氣和氧氣濃度,評估產氫動力學和持續時間。
酶活性和光合作用測量:分析體內外氫酶活性、光系統II(PSII)最大量子產額(F?/F?),并使用抑制劑DCMU驗證產氫對PSII的依賴性。
微環境剖面測繪:使用丹麥Unisense氫微電極和氧微電極,以高空間分辨率(微米級)測量聚集體內部的H?和O?濃度梯度,揭示空間功能分化。
尺寸效應分析:比較不同尺寸聚集體(10 μm、100 μm、500 μm)的產氫效率,確定最優條件。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
產氫定性數據(WO?變色實驗):
數據內容:天然細胞培養液中的WO?顏色不變(無H?),而聚集體培養液中的WO?變為藍灰色,表明有H?生成(濃度約10 μmol L?1)。
研究意義:直觀證明硅化聚集體能在有氧條件下產氫,突破綠藻氫酶的氧敏感限制。數據來自圖1c-e(WO?顏色對比圖)。

產氫定量動力學數據(氣相色譜):
數據內容:在密閉系統中,聚集體以0.35 μmol H? h?1 (mg葉綠素)?1的速率持續產氫至少48小時,而天然細胞無H?生成;O?濃度在聚集體頂空從21%降至19%。
研究意義:定量驗證聚集體的可持續產氫能力,且O?消耗表明呼吸作用創造缺氧微環境。數據來自圖2a(H?和O?隨時間變化曲線)。
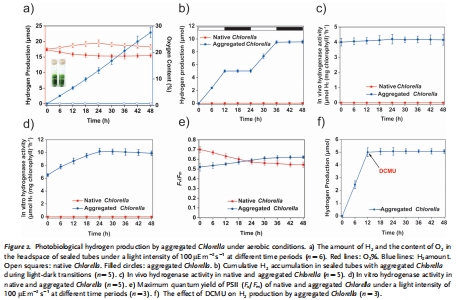
氫酶活性數據:
數據內容:聚集體體內氫酶活性達4 μmol H? h?1 (mg葉綠素)?1(圖2c),體外活性從6.5升至10.3 μmol H? h?1 (mg葉綠素)?1(圖2d),天然細胞無活性。
研究意義:表明硅化處理增強氫酶表達或穩定性,直接關聯產氫能力提升。
光合作用性能數據:
數據內容:聚集體PSII最大量子產額(F?/F?)從0.52升至0.62(圖2e),且DCMU完全抑制產氫(圖2f)。
研究意義:證實產氫依賴PSII的電子傳遞,聚集體維持了光合活性。
微環境剖面數據(使用丹麥Unisense電極測量):
數據內容:在100 μm聚集體中,H?濃度從表面向核心遞增至1.7 μmol L?1,O?濃度從90 μmol L?1降至近零(圖3b)。500 μm聚集體核心H?濃度達5.3 μmol L?1。
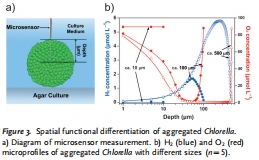
研究意義:直接揭示核殼結構導致空間功能分化—表層細胞耗氧,核心細胞產氫。數據來自圖3b(H?和O?微剖面圖)。
聚集體尺寸效應數據:
數據內容:10 μm聚集體無H?產生;100 μm聚集體產氫效率最優;500 μm聚集體產氫量較低,因PSII活性受損(F?/F?僅0.1–0.3)。
研究意義:表明尺寸調控微環境平衡,過大的聚集體限制光合電子供應。數據來自圖3b和補充圖S9-S12。
研究結論
硅化誘導的細胞聚集體能在自然有氧條件下實現可持續光生物產氫,產氫速率達17 mL H? L?1 culture,比既往報道高9倍。
聚集體核殼結構是關鍵:表層細胞呼吸耗氧,創造核心缺氧微環境,激活氫酶;核心細胞利用光合電子產氫。
產氫依賴PSII活性與氫酶耦合,DCMU抑制實驗證實電子傳遞鏈的必要性。
聚集體尺寸顯著影響效率:100 μm為最優平衡點,過小無缺氧微環境,過大則光合受限。
該策略為綠色能源開發提供了新思路,通過材料-細胞復合體工程調控微生物功能。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense氫微電極和氧微電極測量的數據具有關鍵研究意義,其詳細解讀如下:
高空間分辨率揭示微環境異質性:Unisense微電極是一種電化學傳感器,尖端直徑極細(微米級),能以毫米級空間分辨率原位測量聚集體內部的溶解H?和O?濃度梯度。本研究通過垂直剖面測量(圖3b),直接捕獲了H?濃度從聚集體表面向核心遞增、O?濃度遞減的動態分布。例如,在100 μm聚集體核心,O?濃度近零,而H?濃度達峰值(1.7 μmol L?1),提供了“核殼結構創造缺氧產氫微環境”的最直接證據。這種高精度數據避免了傳統批量測量的空間平均誤差,首次量化了空間功能分化(SFD)的化學基礎。
驗證核殼模型與功能分化機制:微電極數據將理論上的核殼模型轉化為可測量的化學梯度。O?從表層至核心的衰減表明表層細胞呼吸耗氧;H?在核心積累證明產氫活動集中于缺氧區。這強有力地支持了“表層細胞屏蔽氧氣、核心細胞專司產氫”的假說,揭示了聚集體突破氧抑制的物理化學機制。
量化尺寸效應優化設計:通過比較不同尺寸聚集體(10 μm、100 μm、500 μm)的剖面數據,發現100 μm聚集體具有最佳O?-H?梯度平衡:足夠大以形成缺氧核心,但不過大而限制光穿透。Unisense數據為優化聚集體尺寸提供了實證依據,指導了生物反應器設計。
方法學可靠性:Unisense電極的實時響應(秒級)和原位校準確保了數據準確性。其微創測量避免擾動聚集體結構,結果與氣相色譜數據互補,增強了整體結論的可靠性。
總之,丹麥Unisense電極的數據不僅是發現微環境梯度的技術基石,更通過提供高分辨率化學圖譜,將抽象的“空間功能分化”概念轉化為定量規律,凸顯了微傳感器在揭示微生物系統內部機制中的不可替代價值。