熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Characterisation of coral explants: a model organism for cnidarian-dinoflagellate studies
珊瑚外植體的表征:刺胞動物-甲藻研究的模式生物
來源:University of Technology, Sydney, NSW, Australia
論文摘要
本研究通過從造礁石珊瑚Fungia granulosa培養出包含宿主組織和共生甲藻(Symbiodinium)的珊瑚外植體(coral explants),評估了其作為刺胞動物-甲藻共生研究模型生物的可行性。外植體在無骨骼條件下存活超過兩個月,形態學顯示其組織結構(外胚層、中膠層、內胚層)與親本珊瑚相似。光生理學測量表明,一周齡外植體的光合性能(如PSII最大量子產額Fv/FM)與親本珊瑚高度匹配。研究首次通過實證支持珊瑚外植體可作為實驗室模型,用于微觀尺度下宿主-共生體相互作用的分子、遺傳和生理學研究。
研究目的
本研究旨在:
建立并優化珊瑚外植體的培養方法,使其能長期存活并維持生理活性。
表征外植體的形態結構、光生理學特性(如光合效率)和內部微環境(如氧氣、pH梯度)。
比較外植體與親本珊瑚(F. granulosa)的光合性能,驗證其作為共生研究模型的代表性。
利用微傳感器技術量化外植體的代謝活動(如光合作用、呼吸作用),揭示其微觀化學環境特征。
研究思路
研究采用多技術結合的實驗策略:
外植體培養:從F. granulosa珊瑚切割組織楔形塊,經抗生素處理(防止細菌污染)后剝離組織,在無菌玻璃培養皿中培養形成球形外植體(直徑400–800 μm),并添加殼狀珊瑚藻誘導 metamorphosis 線索。
形態學表征:通過光學顯微鏡和熒光顯微鏡觀察外植體的組織分層(外胚層、內胚層、中膠層)及共生甲藻分布,與親本珊瑚結構對比。
光生理學測量:使用脈沖調制熒光成像系統(Imaging PAM)測量外植體和親本珊瑚的穩態光曲線(SSLC),參數包括PSII有效量子產額(ΦPSII)、非光化學淬滅(NPQ)、相對電子傳輸速率(rETR)等。
微環境剖面測量:使用丹麥Unisense氧微電極(Clark型,尖端25 μm)和pH微電極(尖端50 μm)測量外植體在光暗條件下的氧氣和pH垂直剖面(分辨率25–100 μm),并記錄光暗循環(5分鐘間隔)中的氧氣動態響應。
數據比較與分析:將外植體數據與親本珊瑚對比,通過統計檢驗(如t檢驗)評估差異,并關聯形態與生理參數。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
光生理學數據:
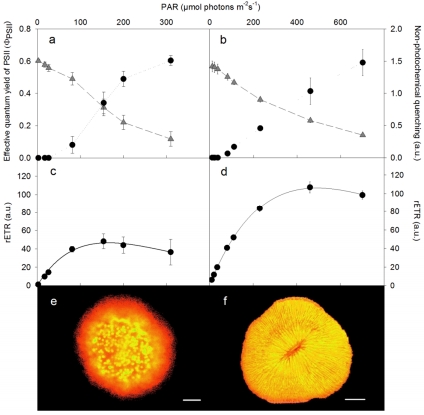
數據內容:外植體和親本珊瑚的SSLC曲線顯示,ΦPSII隨光強(5–313 μmol photons m?2 s?1)增加而下降,NPQ上升;外植體rETR最大值(46.96 ± 8.1)為親本珊瑚(105.55 ± 6.82)的50%,光利用效率(α)更高(0.8 vs. 0.59)。
研究意義:直接證明外植體光生理響應與珊瑚相似,但因生長光強較低(100 vs. 200 μmol photons m?2 s?1)表現出 shade-acclimated 特性(如更高α),驗證了外植體作為光適應研究模型的可行性。數據來自圖2a-d和表1(光參數匯總)。
氧氣和pH微剖面數據(使用丹麥Unisense電極測量):
數據內容:在光下,外植體內部氧氣濃度升高至超氧狀態(最高280 ± 84 μmol L?1),pH升至8.55 ± 0.41;在暗下,氧氣降至112 ± 19 μmol L?1,pH降至7.77 ± 0.09。三分之一外植體無凈氧氣釋放(圖3c)。
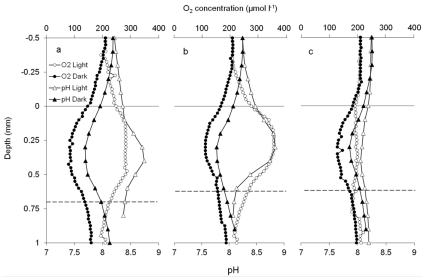
研究意義:首次揭示外植體內部存在化學梯度,光下光合作用產氧增pH,暗下呼吸作用耗氧降pH,模擬了珊瑚組織的微環境動態,證明外植體具有代謝活性。數據來自圖3(光暗剖面對比)。
氧氣動態響應數據:
數據內容:在5分鐘光暗循環中,外植體氧氣濃度在光照后5分鐘內快速上升至穩態(134–368 μmol L?1),暗適應后5分鐘內下降至96–122 μmol L?1(圖4)。響應速度與珊瑚相當。
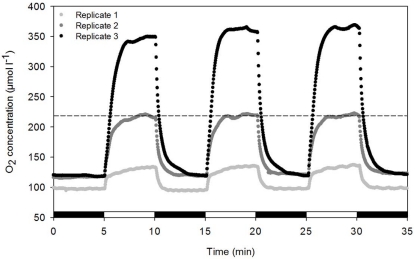
研究意義:表明外植體代謝響應迅速,無缺氧風險(因小尺寸高表面積體積比),支持其作為實時代謝研究模型。數據來自圖4(光暗循環氧氣曲線)。
形態學數據:
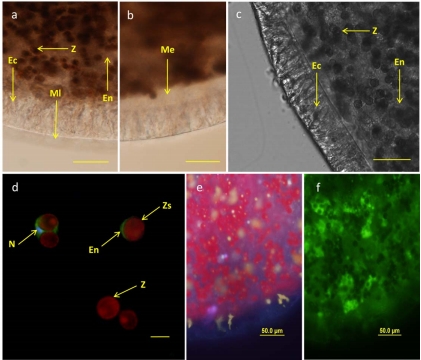
數據內容:顯微鏡圖像顯示外植體具外胚層(帶纖毛和黏液)、內胚層(含共生甲藻)和中膠層,與親本珊瑚結構一致(圖1a-f)。綠色熒光蛋白(GFP)分布異質。
研究意義:證實外植體組織完整性,為宿主-共生體互研提供結構基礎。數據來自圖1。
研究結論
珊瑚外植體是可行的實驗室模型,其形態和光生理學與親本珊瑚高度相似,適合長期(>2個月)共生研究。
外植體光生理參數(如rETR)受生長光強調控,呈現 shade-acclimation 特征,但光合效率(Fv/FM)無顯著差異,表明其適應性強。
微剖面顯示外植體在光下凈自養(產氧增pH),暗下代謝活躍,內部化學梯度與珊瑚一致,驗證其生態相關性。
外植體無骨骼、小尺寸的特性便于微觀操作(如活體成像),為研究宿主-共生體營養轉移、應激響應提供了理想平臺。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense氧和pH微電極測量的數據具有關鍵研究意義,其詳細解讀如下:
高空間分辨率揭示微觀化學環境:Unisense微電極是一種電化學傳感器,尖端極細(氧電極25 μm,pH電極50 μm),能以微米級分辨率無損測量外植體內部的氧氣和pH梯度。本研究通過垂直剖面測量(圖3),直接量化了光下和暗外植體內部的化學異質性。例如,光下pH從外部8.23升至內部8.55,氧氣從飽和值升至280 μmol L?1,提供了共生體光合作用提升微環境pH和氧氣的直接證據,避免了組織勻漿造成的空間信息丟失。
實時動態監測代謝活動:Unisense電極的快速響應(氧電極<2秒)允許記錄光暗循環中氧氣濃度的瞬態變化(圖4)。數據顯示外植體在5分鐘內達到氧平衡,證明其代謝可塑性高,能快速響應光變化。這種實時監測能力將抽象的“代謝活性”轉化為可量化的動力學曲線,為研究環境擾動(如光強波動)對共生的影響提供了工具。
驗證外植體的生態相關性:測量到的化學梯度(光下超氧、暗下低氧)與造礁珊瑚的微環境數據(如Kühl et al. 1995)高度一致,強有力地支持了外植體作為珊瑚共生模型的有效性。例如,pH波動幅度(0.5–0.6單位)模擬了自然珊瑚的晝夜循環,表明外植體可用于研究酸化脅迫下的緩沖機制。
方法學優勢:Unisense電極的原位校準(用硫代硫酸鈉和空氣飽和水校準氧電極,pH緩沖液校準pH電極)確保了數據準確性。其微創測量避免了外植體損傷,結合顯微定位,實現了真實生理狀態下的化學成像。本研究通過對比三個外植體,還揭示了代謝異質性(如一個體無凈氧釋放),突出了個體差異在實驗設計中的重要性。
總之,丹麥Unisense電極的數據不僅是本研究中驗證外植體代謝活性的核心技術證據,更通過提供高分辨率化學剖面,將微觀環境動態與宏觀生理響應鏈接起來,奠定了外植體作為珊瑚共生研究可靠模型的基礎。