熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Seizure-induced reduction in glucose utilization promotes brain hypometabolism during epileptogenesis
癲癇發(fā)作誘導(dǎo)的葡萄糖利用減少促進(jìn)癲癇發(fā)生過程中的腦低代謝
來源:Neurobiology of Disease, Volume 116, 2018, pages 28-38
《神經(jīng)生物學(xué)疾病》,第116卷,2018年,第28-38頁
摘要
這篇論文研究了癲癇發(fā)作如何導(dǎo)致腦葡萄糖低代謝,并探討其在癲癇發(fā)生中的作用。摘要指出,腦葡萄糖低代謝是獲得性癲癇的早期癥狀,其因果機(jī)制尚不清楚。作者提出,癲癇發(fā)作和低代謝之間存在雙向正反饋循環(huán):低代謝誘導(dǎo)癲癇發(fā)作,而癲癇發(fā)作破壞葡萄糖代謝,這可能是獲得性癲癇發(fā)生的主要原因。通過小鼠海馬切片實(shí)驗(yàn),使用4-氨基吡啶誘導(dǎo)癲癇發(fā)作,研究發(fā)現(xiàn)癲癇發(fā)作后會出現(xiàn)持久的葡萄糖低代謝,表明癲癇發(fā)生機(jī)制中可能存在正反饋。癲癇發(fā)作與急性氧化應(yīng)激相關(guān),可能通過H2O2介導(dǎo)代謝受損。外源性丙酮酸,作為線粒體能量底物,能有效正常化癲癇后的葡萄糖消耗,并具有抗癲癇作用。結(jié)果支持代謝概念在癲癇發(fā)生中的機(jī)制,并提供丙酮酸作為潛在治療策略。
研究目的
研究目的是探討癲癇發(fā)作如何導(dǎo)致葡萄糖利用減少和腦低代謝,以及這種低代謝如何促進(jìn)癲癇發(fā)生。具體目標(biāo)是驗(yàn)證癲癇發(fā)作與代謝功能障礙之間的雙向關(guān)系,并研究氧化應(yīng)激和外源性丙酮酸在其中的作用機(jī)制。
研究思路
研究思路采用小鼠海馬切片模型,通過4-氨基吡啶誘導(dǎo)癲癇樣活動,監(jiān)測癲癇發(fā)作前后的電生理和代謝參數(shù)。使用多種測量技術(shù),包括丹麥Unisense電極測量氧氣分壓、酶微電極測量葡萄糖和乳酸濃度、Null傳感器測量H2O2、以及熒光成像監(jiān)測NAD(P)H和FAD變化。實(shí)驗(yàn)比較控制狀態(tài)和癲癇發(fā)作后的代謝狀態(tài),并測試外源性H2O2和丙酮酸的影響,以揭示氧化應(yīng)激和代謝修復(fù)機(jī)制。
測量的數(shù)據(jù)及研究意義
1 數(shù)據(jù):癲癇發(fā)作后葡萄糖消耗減少,表現(xiàn)為刺激誘導(dǎo)的葡萄糖瞬變幅度和積分降低。研究意義:表明癲癇發(fā)作直接抑制葡萄糖利用,可能導(dǎo)致腦低代謝。來源:圖2A。
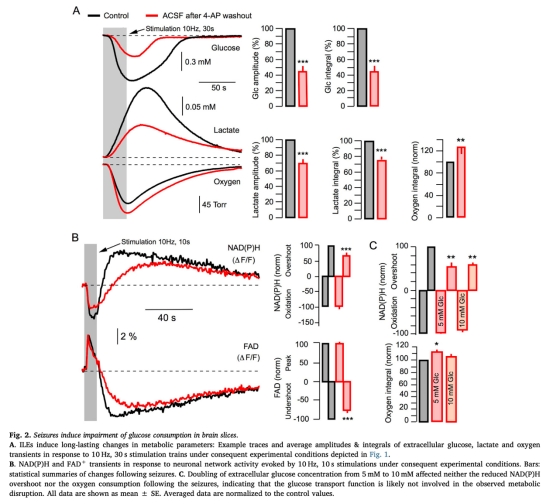
2 數(shù)據(jù):乳酸釋放減少,刺激誘導(dǎo)的乳酸瞬變幅度和積分降低。研究意義:反映糖酵解受阻,支持代謝功能障礙。來源:圖2A。
3 數(shù)據(jù):氧氣消耗增加,盡管葡萄糖利用減少,但氧氣消耗上升。研究意義:表明氧化磷酸化增強(qiáng)或線粒體功能異常,排除缺氧作為原因。來源:圖2A。
4 數(shù)據(jù):NAD(P)H overshoot和FAD undershoot減少。研究意義:指示細(xì)胞質(zhì)糖酵解活性降低,進(jìn)一步證實(shí)代謝受損。來源:圖2B。
5 數(shù)據(jù):H2O2釋放增加,癲癇發(fā)作期間和后H2O2濃度升高。研究意義:表明氧化應(yīng)激參與代謝抑制機(jī)制。來源:圖3。
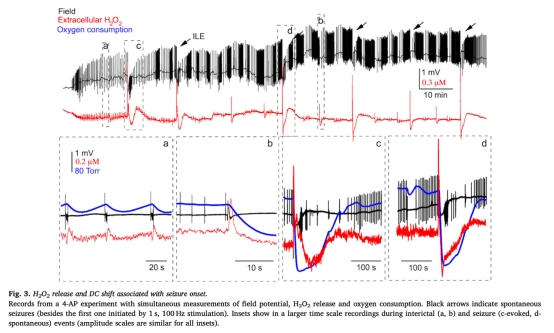
6 數(shù)據(jù):外源性H2O2應(yīng)用模擬癲癇后代謝變化,如葡萄糖利用減少。研究意義:驗(yàn)證氧化應(yīng)激作為關(guān)鍵中介因子。來源:圖4。
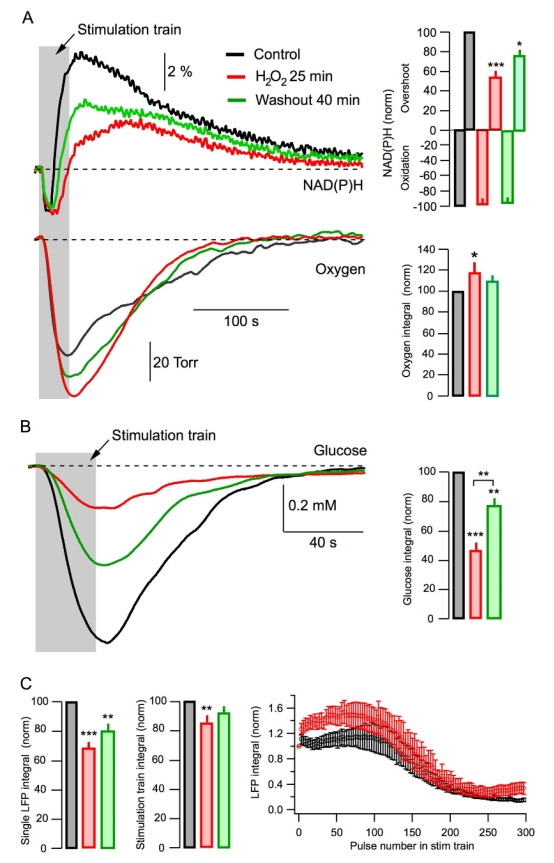

7 數(shù)據(jù):丙酮酸應(yīng)用恢復(fù)葡萄糖利用,正常化代謝參數(shù)。研究意義:表明丙酮酸能逆轉(zhuǎn)癲癇誘導(dǎo)的代謝損傷,提供治療潛力。來源:圖5。
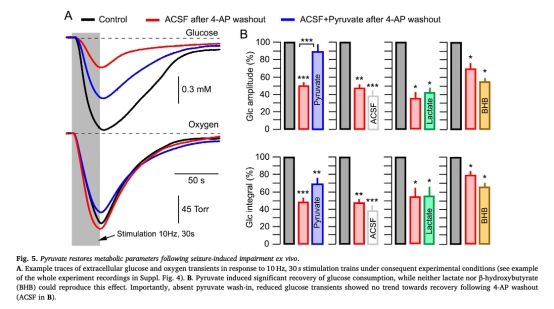
結(jié)論
1 癲癇發(fā)作通過氧化應(yīng)激抑制葡萄糖利用,導(dǎo)致腦低代謝,形成正反饋循環(huán)促進(jìn)癲癇發(fā)生。
2 氧化應(yīng)激主要由H2O2介導(dǎo),直接損傷糖酵解途徑,如GAPDH抑制。
3 外源性丙酮酸能有效恢復(fù)葡萄糖代謝,通過多種機(jī)制包括抗氧化和NAD+再生,打破癲癇發(fā)生的惡性循環(huán)。
使用丹麥Unisense電極測量數(shù)據(jù)的研究意義
丹麥Unisense電極用于測量組織氧分壓(pO2),在研究中顯示癲癇發(fā)作期間pO2下降(從基線約313 mmHg降至188 mmHg),但組織仍保持高氧狀態(tài),未達(dá)到缺氧閾值(通常為10 mmHg)。這些數(shù)據(jù)表明,神經(jīng)血管解耦和微血管損傷不是由組織缺氧引起,因?yàn)閜O2在發(fā)作后迅速恢復(fù),且反復(fù)發(fā)作中pO2響應(yīng)保持穩(wěn)定。相反,pO2測量支持周細(xì)胞線粒體損傷作為主要原因,因?yàn)榫€粒體去極化導(dǎo)致周細(xì)胞收縮和血管功能障礙。Unisense電極的高精度測量提供了關(guān)鍵證據(jù),排除了缺氧作為直接因素,突出了氧化應(yīng)激和代謝功能障礙在癲癇發(fā)生中的核心作用。這有助于理解癲癇相關(guān)腦低代謝的機(jī)制,并指導(dǎo)針對代謝途徑的治療策略。