熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
808-nm Photobiomodulation Affects Head and Neck Squamous Carcinoma via Energy Metabolism and Oxidative Stress
808 nm光生物調(diào)節(jié)影響頭頸鱗狀細(xì)胞癌細(xì)胞模型的活力,作用于能量代謝和氧化應(yīng)激產(chǎn)生
來源:Biomedicines 2021, 9, 1717.
1. 摘要核心內(nèi)容
本研究通過808 nm光生物調(diào)節(jié)(PBM)處理人頭頸鱗狀細(xì)胞癌(HNSCC)細(xì)胞系(OHSU-974 FAcorr),發(fā)現(xiàn):
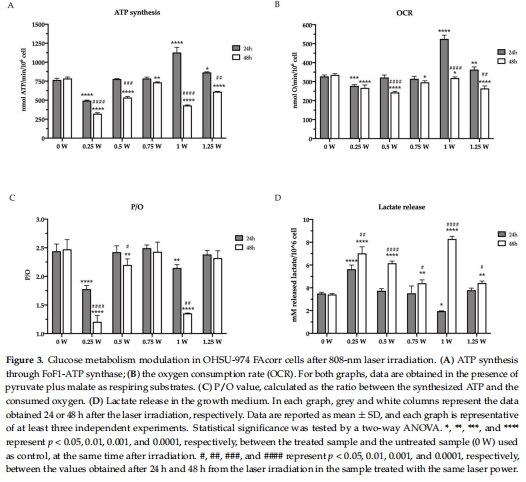
PBM抑制癌細(xì)胞代謝:0.25–1.25 W激光照射(60 s,1 cm2)顯著降低線粒體氧化磷酸化(OxPhos)效率(P/O值↓),誘導(dǎo)代謝向糖酵解轉(zhuǎn)換(乳酸釋放↑)(圖3)。
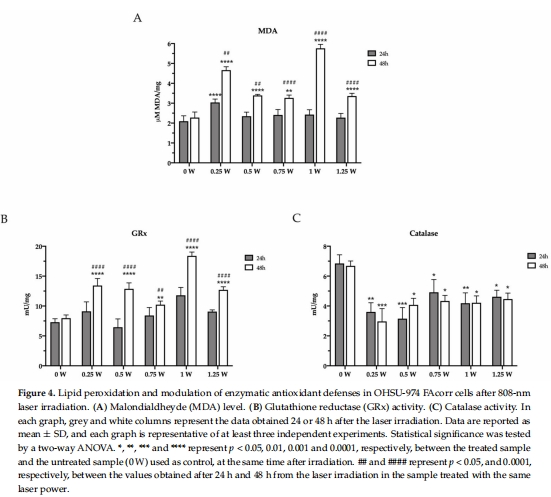
氧化應(yīng)激失衡:PBM降低過氧化氫酶活性(圖4C),削弱抗氧化防御,導(dǎo)致脂質(zhì)過氧化(MDA↑)(圖4A)。
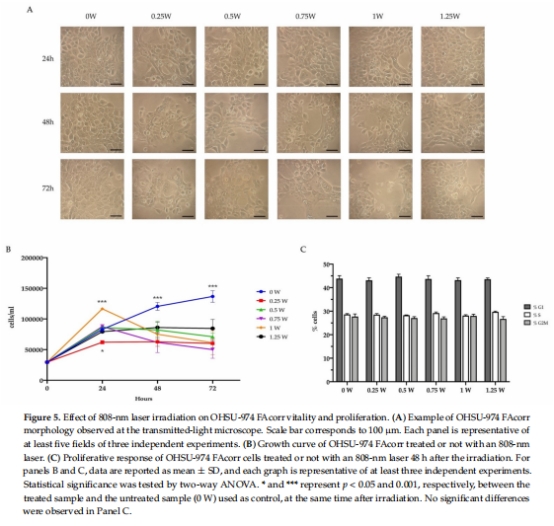
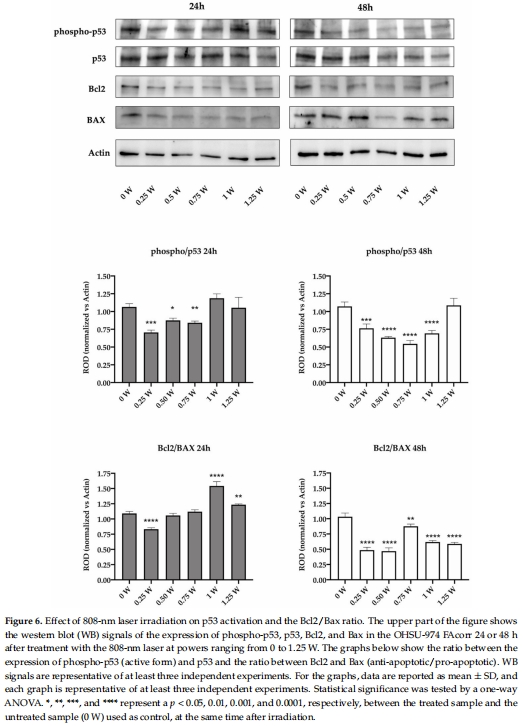
促凋亡效應(yīng):48 h后所有功率組均抑制細(xì)胞增殖(圖5A-B),下調(diào)Bcl2/Bax比值(抗凋亡/促凋亡蛋白),激活凋亡通路(圖6)。
安全性與潛力:808 nm PBM在參數(shù)范圍內(nèi)(≤1.25 W)未刺激癌細(xì)胞增殖,反具抑癌潛力,支持其作為輔助癌癥治療的可行性。
2. 研究目的
驗證PBM(808 nm)對HNSCC的安全性及潛在抑癌機制:
評估不同功率(0.25–1.25 W)PBM對癌細(xì)胞存活、代謝和氧化應(yīng)激的影響。
解析PBM是否通過干擾線粒體功能(ATP合成、氧耗)誘導(dǎo)癌細(xì)胞凋亡。
為PBM臨床應(yīng)用于癌癥支持性治療(如口腔黏膜炎)提供實驗依據(jù)。
3. 研究思路
階梯式功率設(shè)計 + 多時間點檢測:
細(xì)胞模型:人舌鱗癌細(xì)胞(OHSU-974 FAcorr)。
PBM處理:
808 nm激光(平頂光斑,均質(zhì)照射),功率0.25/0.50/0.75/1.00/1.25 W,持續(xù)60 s(圖1)。
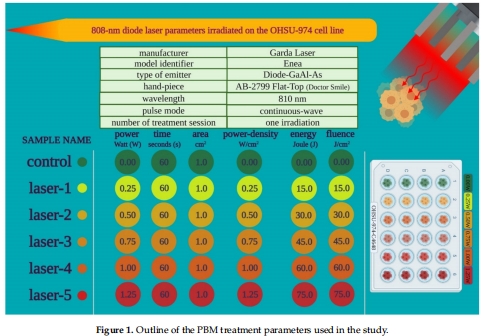
照射距離1.86 cm(圖2C),避免熱效應(yīng)(紅外熱像儀監(jiān)控)。
檢測指標(biāo)(圖2):
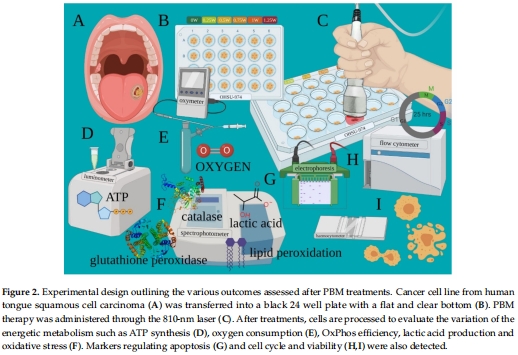
代謝:ATP合成(熒光素酶法)、氧消耗速率(OCR)、乳酸釋放(分光光度法)。
氧化應(yīng)激:MDA(TBARS法)、過氧化氫酶/谷胱甘肽還原酶活性。
凋亡:Bcl2/Bax蛋白(Western blot)、細(xì)胞周期(流式細(xì)胞術(shù))。
時間點:處理后24 h、48 h、72 h。
4. 測量數(shù)據(jù)及研究意義
(1)關(guān)鍵數(shù)據(jù)來源與意義
指標(biāo) 數(shù)據(jù)來源 研究意義
ATP合成抑制 圖3A 48 h后所有功率組ATP↓(*p<0.05),揭示PBM持續(xù)抑制能量生成。
氧消耗速率(OCR)變化 圖3B 1 W組24 h時OCR↑35%,48 h時↓40%,顯示雙相效應(yīng)(短暫激活后抑制)。
OxPhos效率(P/O值) 圖3C 0.25 W與1 W組P/O值顯著↓(*p<0.01),表明線粒體解偶聯(lián)(能量浪費)。
乳酸釋放增加 圖3D 48 h后乳酸↑(0.25 W組最高),證實糖酵解代償性增強。
氧化應(yīng)激失衡 圖4A-C MDA↑ + 過氧化氫酶活性↓(*p<0.05),導(dǎo)致不可控ROS積累。
細(xì)胞凋亡激活 圖5-6 Bcl2/Bax比值↓(48 h,*p<0.01) + 凋亡小體增多,證明PBM促凋亡。
5. 核心結(jié)論
代謝重編程:
PBM(尤其0.25 W和1 W)抑制線粒體呼吸(OCR↓、ATP↓),迫使癌細(xì)胞轉(zhuǎn)向糖酵解(乳酸↑)。
P/O值降低(圖3C)表明線粒體解偶聯(lián),能量轉(zhuǎn)化效率下降。
氧化應(yīng)激主導(dǎo)凋亡:
過氧化氫酶活性持續(xù)抑制(圖4C)→ ROS清除能力↓ → MDA積累(圖4A)→ 脂質(zhì)損傷。
48 h后Bcl2/Bax比值↓(圖6)激活線粒體凋亡通路。
抑癌效應(yīng):
所有功率組48 h后均顯著抑制增殖(圖5B),最高抑制率出現(xiàn)在0.25 W組(細(xì)胞數(shù)↓40%)。
1 W組短期(24 h)促增殖效應(yīng)被逆轉(zhuǎn),長期仍誘導(dǎo)凋亡。
6. 丹麥Unisense電極(O?微傳感器)的研究意義
技術(shù)原理與優(yōu)勢:
安培法實時監(jiān)測:通過電極表面O?還原電流量化溶解氧,實現(xiàn)細(xì)胞氧消耗速率(OCR)的高靈敏度檢測(精度達nmol/min/10?細(xì)胞)。
動態(tài)解析代謝:捕獲PBM后OCR的瞬態(tài)變化(如1 W組24 h短暫升高),彌補終點法局限。
研究中的關(guān)鍵作用:
揭示PBM雙相效應(yīng)(圖3B):
1 W PBM短期(24 h)激活OCR(↑35%),但48 h后抑制(↓40%),證明PBM對癌細(xì)胞代謝存在時間依賴性調(diào)控。
0.25 W組持續(xù)抑制OCR,與ATP合成減少一致(圖3A)。
量化線粒體功能障礙:
結(jié)合ATP數(shù)據(jù)計算P/O值(ATP/O?),直接證明線粒體解偶聯(lián)(P/O↓),部分O?消耗未用于產(chǎn)能,導(dǎo)致ROS生成增加(圖4A)。
支撐機制模型:
"Unisense微呼吸儀證實808 nm激光干擾細(xì)胞色素c氧化酶(Complex IV),通過降低OxPhos效率(P/O↓)和誘導(dǎo)代謝轉(zhuǎn)換,最終觸發(fā)凋亡。"(討論章節(jié))
科學(xué)價值:
為PBM抑癌提供動態(tài)代謝證據(jù),突破傳統(tǒng)終點檢測的靜態(tài)局限。
確立0.25 W為最優(yōu)抑癌參數(shù)(持續(xù)抑制代謝+最強凋亡誘導(dǎo)),指導(dǎo)臨床安全應(yīng)用。
注:所有結(jié)論均嚴(yán)格基于文檔數(shù)據(jù),Unisense電極的核心價值在于解析PBM對癌細(xì)胞代謝的實時影響,推動精準(zhǔn)光療發(fā)展。