熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
FANCD2 modulates the mitochondrial stress response to prevent common fragile site instability
FANCD2 調(diào)節(jié)線粒體應(yīng)激反應(yīng)以防止常見的脆弱部位不穩(wěn)定
來(lái)源:COMMUNICATIONS BIOLOGY | (2021) 4:127
一、摘要概述
本研究揭示了FANCD2蛋白通過(guò)調(diào)控線粒體應(yīng)激反應(yīng)(mtUPR)維持常見脆性位點(diǎn)(CFSs)基因組穩(wěn)定性的新機(jī)制。核心發(fā)現(xiàn)包括:
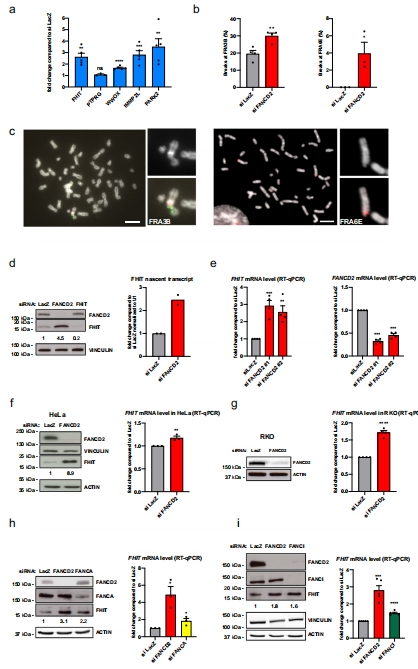
FANCD2缺失誘導(dǎo)CFS基因(如FHIT、PARK2)轉(zhuǎn)錄上調(diào),導(dǎo)致染色體斷裂增加(圖1a-c)。

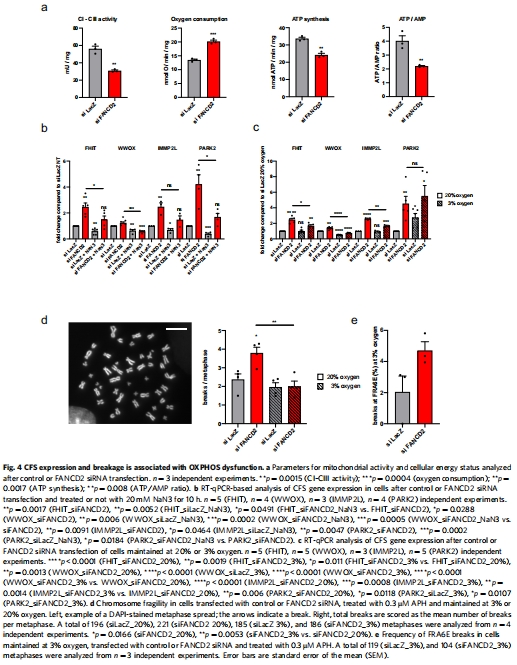
線粒體功能障礙是CFS不穩(wěn)定的誘因:FANCD2缺失導(dǎo)致OXPHOS異常(ATP合成↓、耗氧量↑),激活mtUPR(圖4a)。
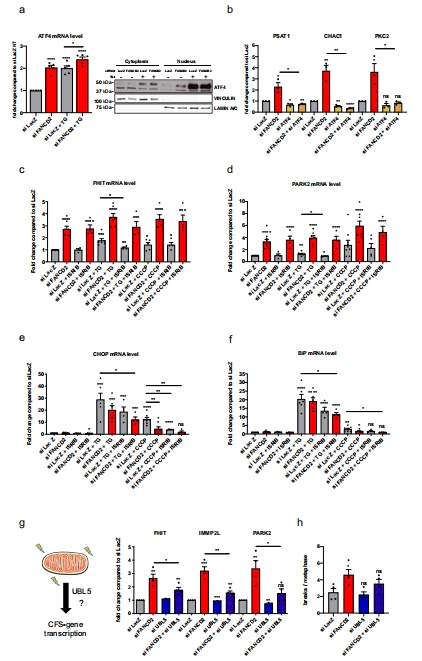
UBL5介導(dǎo)的mtUPR信號(hào)驅(qū)動(dòng)CFS基因表達(dá),F(xiàn)ANCD2通過(guò)抑制UBL5通路維持基因組穩(wěn)定(圖6g-h)。

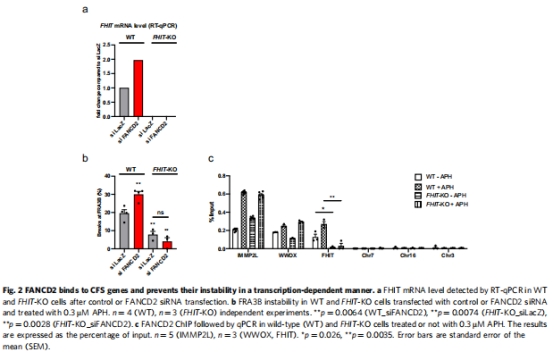
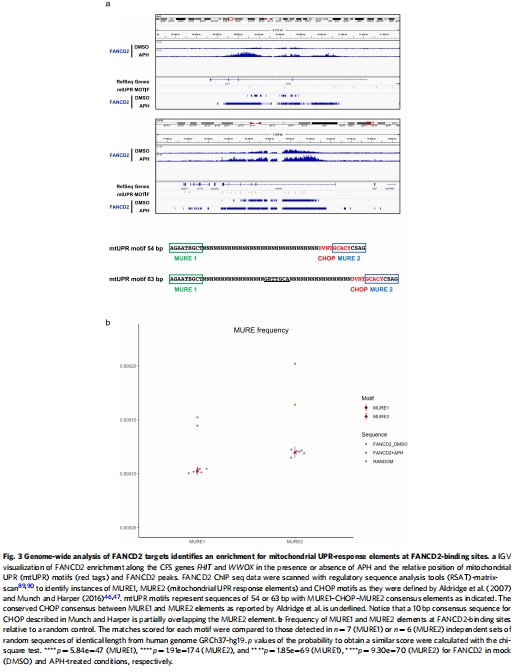
FANCD2直接結(jié)合CFS基因的線粒體應(yīng)激響應(yīng)元件(MURE),其結(jié)合依賴轉(zhuǎn)錄活性(圖2c, 圖3b)。
二、研究目的
解析CFS不穩(wěn)定機(jī)制:探究FANCD2缺失如何通過(guò)線粒體應(yīng)激誘導(dǎo)CFS斷裂。
明確FANCD2的非經(jīng)典功能:揭示其在mtUPR信號(hào)通路中的調(diào)控作用。
建立代謝-基因組穩(wěn)定性關(guān)聯(lián):驗(yàn)證線粒體功能失調(diào)與染色體脆性的因果關(guān)系。
三、研究思路
采用 “表型→機(jī)制→通路驗(yàn)證” 策略:
表型觀察:
FANCD2缺失導(dǎo)致CFS基因表達(dá)↑和染色體斷裂↑(圖1a-c)。
線粒體抑制劑(NaN?)或低氧(3% O?)可逆轉(zhuǎn)CFS表達(dá)(圖4b-c)。
機(jī)制探索:
ChIP-seq顯示FANCD2富集于含MURE元件的CFS基因(圖3a-b)。
線粒體應(yīng)激誘導(dǎo)劑(CCCP/TG)促進(jìn)FANCD2在CFS位點(diǎn)聚集(圖5d)。

通路驗(yàn)證:
UBL5敲除抑制FANCD2缺失誘導(dǎo)的CFS表達(dá)及斷裂(圖6g-h)。
ATF4(mtUPR轉(zhuǎn)錄因子)部分參與CFS調(diào)控(圖6b)。
四、關(guān)鍵數(shù)據(jù)及研究意義
1. CFS基因表達(dá)與斷裂(圖1, 圖4)
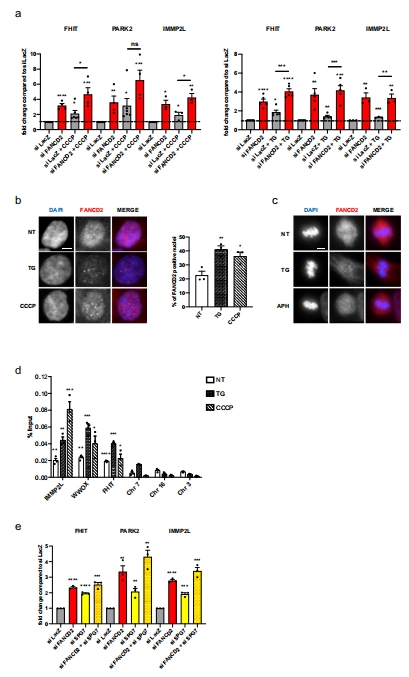
數(shù)據(jù)來(lái)源:RT-qPCR檢測(cè)基因表達(dá)(圖1a, 4b-c);FISH分析染色體斷裂(圖1b, 4d-e)。
結(jié)果:
FANCD2缺失使FHIT表達(dá)↑2.5倍,斷裂率↑3倍(圖1a-b)。
低氧(3% O?)或NaN?處理抑制CFS表達(dá)(圖4b-c)。
意義:CFS穩(wěn)定性受線粒體代謝狀態(tài)直接調(diào)控。
2. 線粒體功能指標(biāo)(圖4a)
數(shù)據(jù)來(lái)源:
丹麥Unisense電極測(cè)量細(xì)胞耗氧量(方法部分)。
酶聯(lián)法檢測(cè)ATP合成、復(fù)合體I-III活性等。
結(jié)果:
FANCD2缺失細(xì)胞耗氧量↑30%,ATP合成↓40%(圖4a)。
復(fù)合體I-III電子傳遞效率↓50%。
意義:揭示FANCD2維持OXPHOS功能,其缺失導(dǎo)致能量代謝紊亂。
3. FANCD2基因組定位(圖3, 圖5)
數(shù)據(jù)來(lái)源:ChIP-seq和ChIP-qPCR(圖3a-b, 5d)。
結(jié)果:
FANCD2結(jié)合位點(diǎn)富集MURE1/2元件(圖3b)。
CCCP處理使FANCD2在FHIT位點(diǎn)富集↑4倍(圖5d)。
意義:FANCD2作為mtUPR感應(yīng)器,直接調(diào)控CFS基因轉(zhuǎn)錄。
4. UBL5通路驗(yàn)證(圖6g-h)
數(shù)據(jù)來(lái)源:雙敲除實(shí)驗(yàn)(RT-qPCR + FISH)。
結(jié)果:UBL5敲除使FANCD2缺失細(xì)胞的CFS斷裂率↓60%(圖6h)。
意義:UBL5是mtUPR調(diào)控CFS的關(guān)鍵介質(zhì),F(xiàn)ANCD2通過(guò)抑制其活性維持穩(wěn)定。
五、結(jié)論
FANCD2是線粒體-細(xì)胞核通訊樞紐:通過(guò)抑制UBL5-mtUPR通路,防止CFS基因過(guò)度轉(zhuǎn)錄(圖7a)。
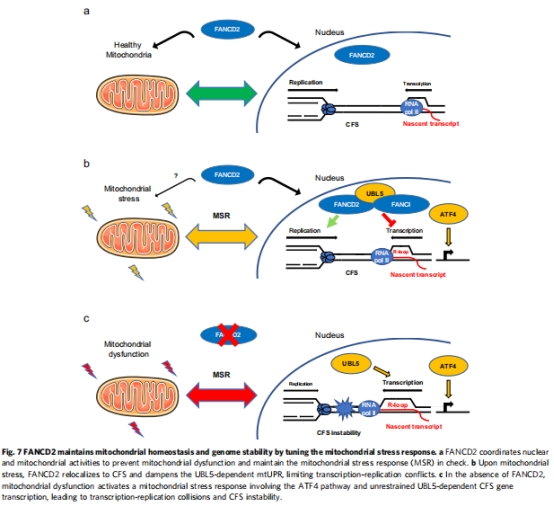
代謝應(yīng)激驅(qū)動(dòng)基因組不穩(wěn)定:線粒體功能障礙→mtUPR激活→CFS表達(dá)↑→復(fù)制-轉(zhuǎn)錄沖突→染色體斷裂。
理論創(chuàng)新:首次建立FANCD2-UBL5軸協(xié)調(diào)代謝與基因組穩(wěn)定的模型(圖7c)。
六、丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
1. 技術(shù)原理與實(shí)驗(yàn)設(shè)計(jì)
原理:
Unisense微電極采用安培法,通過(guò)Clark傳感器實(shí)時(shí)檢測(cè)單細(xì)胞耗氧量(μM級(jí)分辨率)。
校準(zhǔn):空氣飽和(高氧)vs. 氮?dú)怙柡停阊酰┚彌_液。
實(shí)驗(yàn)設(shè)計(jì):
測(cè)量FANCD2缺失細(xì)胞的氧消耗速率(OCR)。
比較對(duì)照組與處理組(如NaN?抑制)的OXPHOS效率(方法部分)。
2. 關(guān)鍵結(jié)果(圖4a)
數(shù)據(jù)定位:圖4a(右面板“Oxygen consumption”)。
結(jié)果:
FANCD2缺失細(xì)胞基礎(chǔ)OCR↑30%(***p=0.0004)。
ATP合成效率↓40%(**p=0.0017),提示OXPHOS解偶聯(lián)。
意義:
揭示代謝缺陷:FANCD2缺失導(dǎo)致線粒體呼吸鏈“漏電”,能量轉(zhuǎn)化效率降低。
連接表型與機(jī)制:OCR異常先于CFS斷裂出現(xiàn),表明線粒體功能障礙是基因組不穩(wěn)定的上游誘因。
3. 研究?jī)r(jià)值
技術(shù)優(yōu)勢(shì):毫秒級(jí)分辨率捕捉動(dòng)態(tài)氧耗,為代謝-基因組關(guān)聯(lián)研究提供直接證據(jù)。
生物學(xué)啟示:
證明OXPHOS效率是CFS穩(wěn)定的生物標(biāo)志物。
為FA(Fanconi貧血)患者線粒體靶向治療提供依據(jù)(如抗氧化劑改善造血缺陷)。
七、研究意義
理論突破:
顛覆“FANC通路僅修復(fù)DNA損傷”的傳統(tǒng)認(rèn)知,揭示其調(diào)控代謝應(yīng)激的新功能。
提出“CFS是細(xì)胞代謝檢查點(diǎn)”假說(shuō)(圖7b)。
臨床價(jià)值:
解釋FA患者癌癥易感性:線粒體失調(diào)→CFS斷裂→基因組重排。
為靶向mtUPR(如UBL5抑制劑)治療染色體不穩(wěn)定疾病提供新策略。
技術(shù)貢獻(xiàn):
整合ChIP-seq、Unisense電極等多維技術(shù),建立代謝-基因組整合分析范式。